2025年10月11日,康宁杰瑞宣布,其自主研发的注射用 JSKN022 已获CDE的临床试验默示许可,用于晚期实体肿瘤患者的首例人体给药研究。
图源:CDE 官网
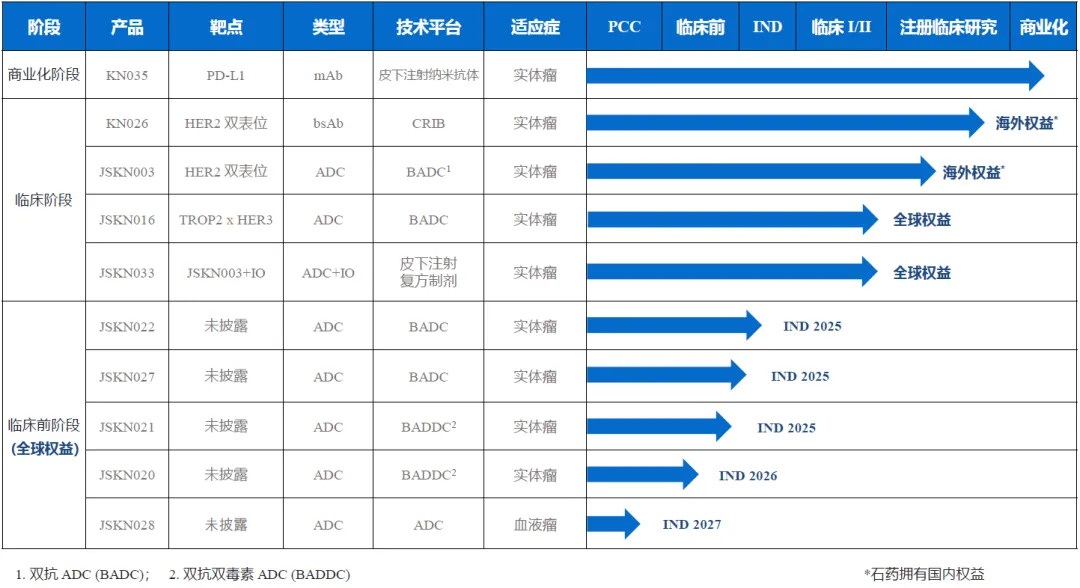
JSKN022 是公司基于糖基定点偶联技术平台打造的一款创新型双特异性抗体偶联药物(ADC),能够同时识别肿瘤细胞表面的 PD-L1 与整合素 αvβ6。药物与任一靶点结合后,通过靶点介导的内吞进入细胞内,在溶酶体中可裂解的连接子在蛋白水解酶作用下释放出具细胞毒性的拓扑异构酶 I 抑制剂(T01)。这一设计既能直接诱导抗原阳性细胞的凋亡,又可发挥旁观者效应,对抗原阴性细胞也具备杀伤能力,从而实现双重肿瘤抑制机制。点击了解PD-L1/ αvβ6相关产品
在 2025 年 AACR 年会上披露的临床前数据中,JSKN022 在体外与体内模型中表现出显著的抗肿瘤活性。它不仅可特异结合 PD-L1、αvβ6 及 αvβ8,且几乎无交叉识别其他整合素家族成员;在 HCC4006 与 Capan-2 细胞系中,其内吞效率优于单靶点抗体;在动物模型中,对阳性肿瘤的抑制效果也显著强于单靶点 ADC。此外,得益于糖基定点偶联技术,JSKN022 在不同物种血清中均表现出极低的 T01 自发释放率,显示出优异的稳定性。
公司计划于 2025 年内在中国启动该药物在标准治疗失败的晚期实体瘤患者中的 I 期临床研究,以评估其安全性、耐受性、药代动力学/药效学特征,并探索最大耐受剂量(MTD)或推荐 II 期剂量(RP2D)。
目前,全球尚无针对 αvβ6 或 PD-L1 的 ADC 药物获批上市,相关项目仍处于临床阶段。康宁杰瑞表示,JSKN022 有望成为全球首款真正意义上的 PD-L1/αvβ6 双抗 ADC,并可能为 PD-1/PD-L1 抑制剂耐药或疗效不佳的晚期实体瘤患者(如非小细胞肺癌、头颈部鳞癌、结直肠癌等)提供新的治疗选择。
除 JSKN022 外,康宁杰瑞还在研多个双抗 / ADC 产品线,其中包括 HER2 双抗 ADC(JSKN003)、靶向 HER3 与 TROP2 的双抗 ADC(JSKN016)、EGFR/HER3 双抗双载荷 ADC(JSKN021)等。