10月8日,宜联生物宣布,与安进达成全球临床研究和药品供应合作协议。安进将主导一项全球临床研究,以评估宜联生物的靶向B7-H3抗体偶联药物YL201与其靶向DLL3和CD3的双特异性T细胞衔接蛋白(BiTE®)IMDELLTRA™联合治疗广泛期小细胞肺癌(ES-SCLC)的潜力。宜联生物将为该联合研究提供试验性药物YL201。
这项全球多中心、开放标签的Ib期临床试验旨在评估YL201与IMDELLTRA™的联合用药在ES-SCLC患者中的安全性、耐受性、药代动力学和疗效。YL201和IMDELLTRA™都已在ES-SCLC领域展现出潜力。
IMDELLTRA™是安进公司研发的一款first-in-class靶向免疫疗法,它能够同时结合肿瘤细胞上的 DLL3 和 T 细胞上的CD3,激活 T 细胞形成细胞溶解突触并杀伤DLL3表达的SCLC细胞。DLL3 表达在 ~85-96% 的 SCLC 患者肿瘤细胞表面,但极少在健康细胞上表达,这样的表达量差异使得DLL3成为诊疗SCLC的潜力靶点。
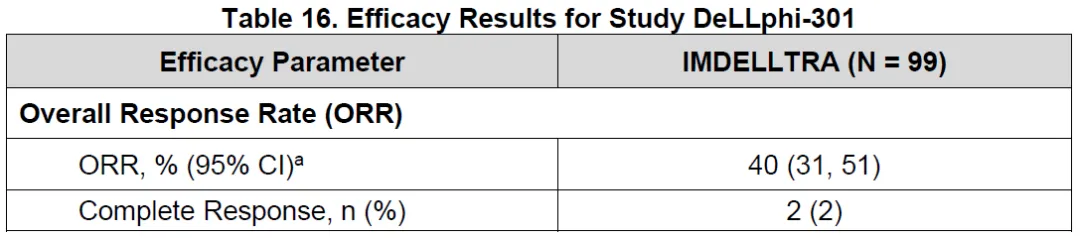
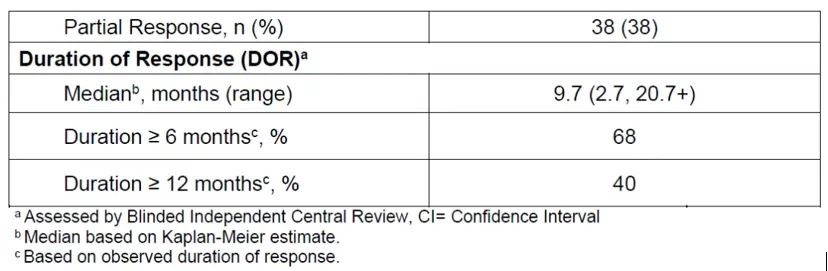
今年5月IMDELLTRA™已获得FDA加速批准用于治疗接受含铂化疗时或接受含铂化疗治疗后进展的ES-SCLC成人患者。该适应症的加速批准是基于ORR和DoR数据,该适应症的完全批准将有赖于在确证性试验中进一步验证和明确其临床疗效。目前,IMDELLTRA™已在美国市场进行商业化销售。
YL201是宜联公司成立后的首发项目,在ES-SCLC中也已展现出优异疗效。9月13日,宜联生物在2024 ESMO大会上首次公布了B7H3 ADC YL201用于包括SCLC在内的晚期实体瘤患者的I/II期临床试验结果。
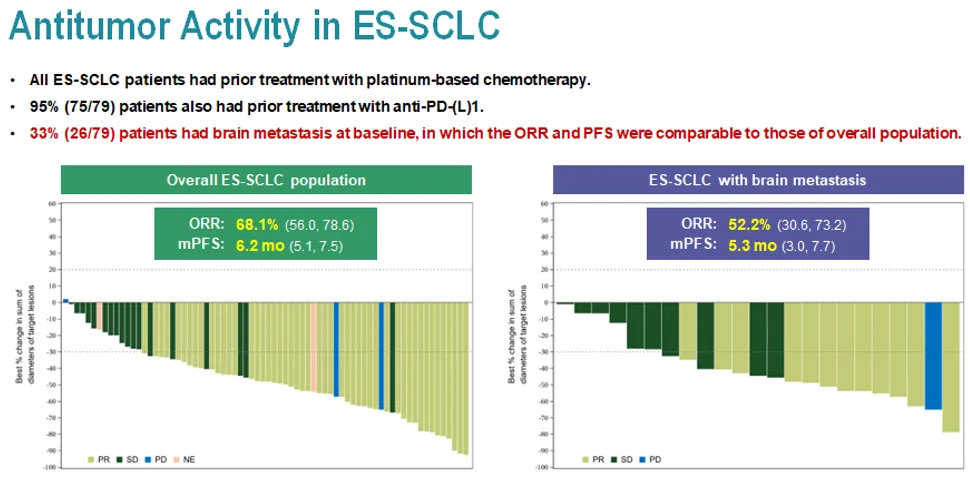
有效性方面,截至2024年8月9日,在276例存在至少一次基线后肿瘤评估的患者中,客观缓解率(ORR)为44.6%,疾病控制率(DCR)为83.7%。在多种实体瘤类型中观察到抗肿瘤活性。在大分期SCLC患者中,在72例可评估肿瘤的患者中,所有患者之前都接受过铂类化疗,95%的患者之前接受过抗PD-(L)1治疗。ORR为68.1%(剂量水平>= 2.0 mg/kg: 70.0%),中位无进展生存期(mPFS)为6.2个月(剂量水平>= 2.0 mg/kg: 6.2个月)。另外值得一提的是,脑转移患者的ORR为52.2%,mPFS为5.3个月,与总体人群相当。
值得一提的是,宜联生物于9月25日在Clinicaltrials.gov网站上登记了一项评估 YL201在复发性小细胞肺癌中的疗效和安全性的 III 期临床研究试验。这是一项多中心、随机、对照、开放标签、III 期研究,旨在比较 YL201与托泊替康在复发性小细胞肺癌(SCLC) 受试者中的疗效和安全性。该研究计划入组438例复发性小细胞肺癌患者,预计2027年底初步完成。
本次联用合作将探索两款创新药物在ES-SCLC治疗中的潜力,通过YL201与IMDELLTRA™的潜在协同作用从而有望进一步提高临床获益。
吉满生物可提供B7H3/B7H4表达细胞系,用于抗体药物的筛选,(点击了解产品,咨询吉满客服联系同微信:18916119826)