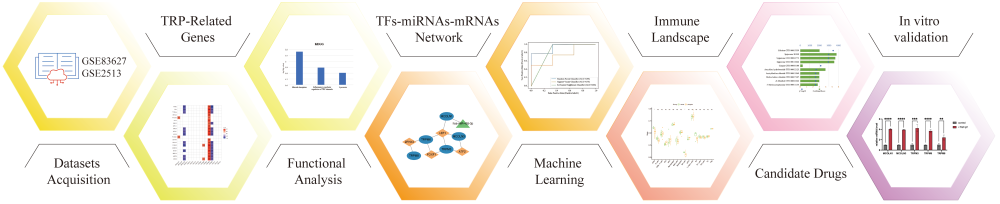
近日,上海交通大学附属第九人民医院眼科在Inflammation Research(IF=6.986)杂志发表题为“Uncovering the Role of Transient Receptor Potential Channels in Pterygium: A Machine Learning Approach”研究性论文,傅瑶教授为本文通讯作者,蔡雨宸博士是该文第一作者,周天一博士是共同一作。该研究发现TRP通道在翼状胬肉的发病机制中发挥了重要作用,基于多个机器学习程序,构建并验证了翼状胬肉的5个TRP基因特征(MCOLN1、MCOLN3、TRPM3、TRPM6和TRPM8),功能分析证明了TRP通道参与炎症调节和溶酶体相关途径,并通过体外实验进一步验证了结果的可靠性。该研究所发现的关键生物标志物和通路为未来翼状胬肉的机制和治疗研究提供了新的方向。
翼状胬肉是一种发病率极高的眼表慢性炎症性疾病,该疾病具有损伤视力的风险;作为一种结膜病理性的过度生长,其发生伴随着新生血管的形成和慢性炎症。但由于发病机制尚不清楚,即使通过手术干预恢复视力之后,预防术后复发也具有一定的挑战性。因此,需要发现新的生物标志物来解释翼状胬肉的发病机制和探索新的治疗方法。瞬时受体电位(TRP)通道是一种广泛存在于体内的阳离子通道,通过影响阳离子浓度的变化,TRP通道改变细胞内相应通路信号的强度,导致细胞功能的改变。TRP通道超家族参与各种生理和病理过程,越来越多的报道支持它们在炎症反应、细胞迁移、血管生成等过程中的作用。
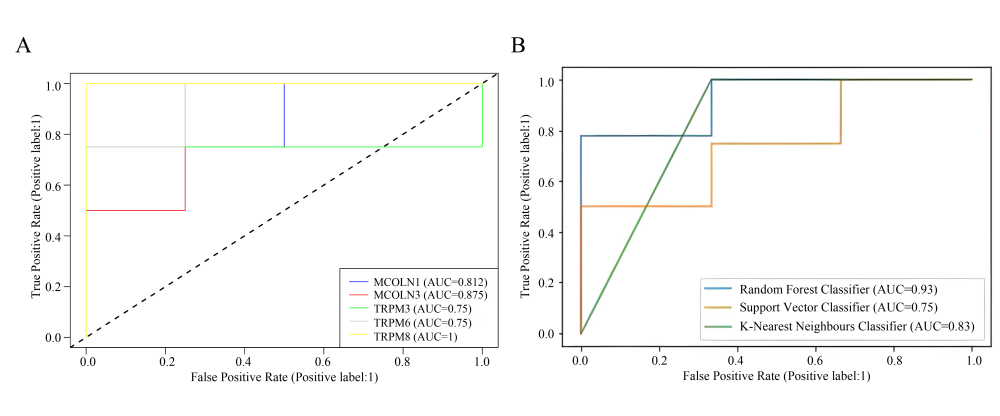
在本工作中,研究者利用生物信息学方法,筛选出TRP相关基因(MCOLN1、MCOLN3、TRPM3、TRPM6和TRPM8),并应用三种机器学习算法(支持向量机、随机森林和k近邻法)来验证相应的TRP翼状胬肉的预测特征。
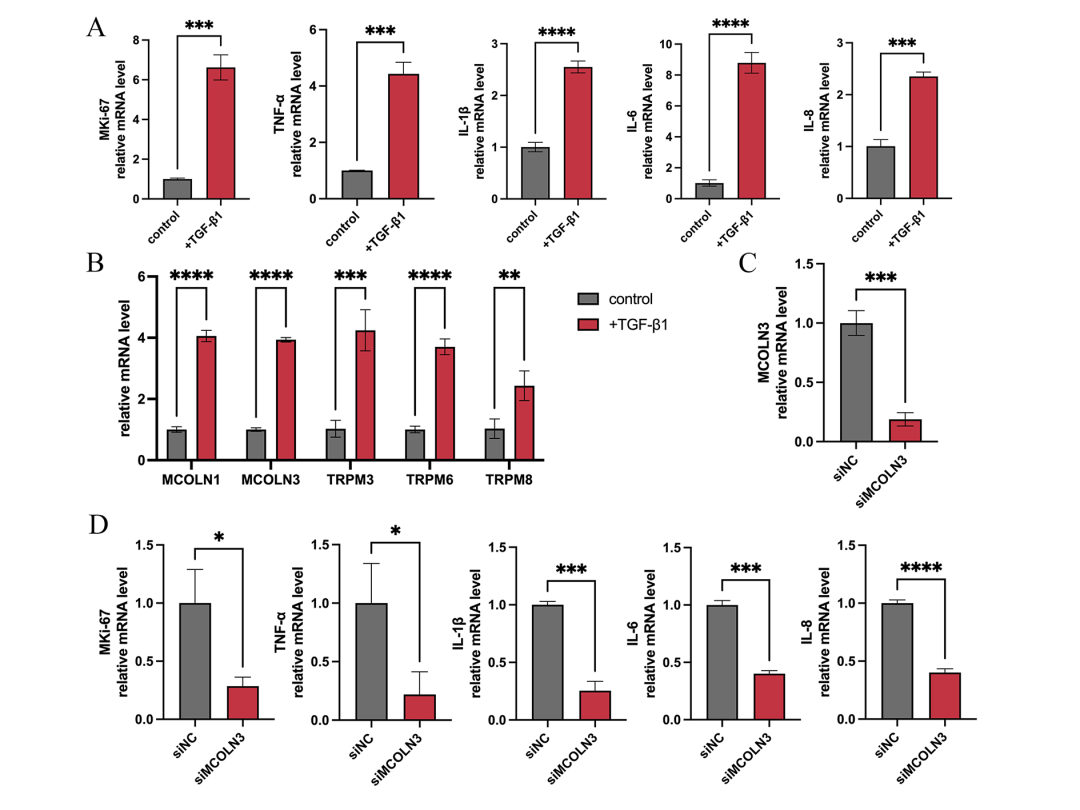
最后,研究者使用人原代结膜上皮细胞进行体外验证。首先,使用TGF-β1模拟翼状胬肉的细胞模型。为了验证TGF-β1对人结膜上皮的诱导作用,进行RT-PCR检测增殖标志物MKi67和促炎症细胞因子(TNF-α、IL-1β、IL-6和IL-8)的mRNA表达。结果表明,TGF-β1处理结膜上皮细胞后,增殖和促炎症标志物都明显上调。同时,5个TRP相关基因(MCOLN1、MCOLN3、TRPM3、TRPM6和TRPM8)的表达水平在TGF-β1处理后明显增加,意味着这5个TRP相关基因在翼状胬肉的增殖和炎症过程中可能发挥重要作用。由于MCOLN3在计算机模拟分析中被确定为最有希望的生物标志物,研究者进一步在结膜上皮中进行siRNA靶向敲除以验证其潜在功能。研究者发现在结膜上皮细胞中敲除MCOLN3后,增殖标志物MKI67和促炎症细胞因子TNF-α、IL-1β、IL-6和IL-8水平明显下调。这一结果表明MCOLN3能够影响结膜组织的增殖和促炎症信号,从而导致翼状胬肉的发生。
本研究首次阐明了TRP通道在翼状胬肉发病中的关键作用。近年来靶向TRP通道的药物研究正逐渐增多,可据此开发抗炎药物、研究相关的离子通道疾病,具有广阔前景。目前TRP通道在许多眼表疾病中的具体作用机制尚未完全明确,未来还需对TRP通道各亚型在眼表不同类型细胞中的调控机制、TRP通道靶向药物在疾病模型与实际临床疾病中应用的差异等问题进行更加深入的研究。
吉满助力
本实验所用MCOLN3-targeting short interfering RNAs (siRNAs)由吉满生物(Genomeditech)提供。了解更多质粒构建、病毒包装、稳转株构建、CRISPR/Cas9、报告基因检测等相关服务。
欢迎访问吉满生物官方网站:www.genomeditech.com
联系电话:4006279288