研究背景
头颈部鳞状细胞癌 (HNSCC)是头颈部常见的恶性肿瘤,每年新增病例超过70万。常见治疗方法包括手术、放疗、化疗、靶向治疗、免疫治疗等。在靶向治疗中,尽管90%的HNSCC患者具有高EGFR表达,但EGFR的靶向药——西妥昔单抗的治疗效果仍不理想。其耐药机制可能与EGFR和RAS突变、间质-上皮转化及其他途径激活有关。此外,表观遗传调控也可能是调控耐药的关键途径。
微小核糖核酸(miRNAs) 在许多疾病的发展中起重要作用,包括西妥昔单抗耐药[15-17]。通常认为miRNAs通过靶向信使RNA的3'-非翻译区,在细胞质中负向调控基因表达。但一些研究表明miRNAs也可通过RNA激活(RNAa)机制在细胞核中促进基因表达。因此,了解miRNAs核内调控机制,可能补充对miRNA的功能的理解,同时为解决西妥昔单抗耐药提供新的解决思路。
文献来源
近日,上海交通大学医学院附属第九人民医院的郭海艳、张建军在Cellular and Molecular Life Sciences上发表了题为“Nuclear miR 451a activates KDM7A and leads to cetuximab resistance in head and neck squamous cell carcinoma” 的研究论文。
该研究发现,miR-451a在西妥昔单抗耐药细胞核中富集,并通过由AGO2介导的增强子-miRNA相互作用靶向并激活KDM7A基因,促进西妥昔单抗耐药。研究证实了miR-451a和KDM7A在西妥昔单抗耐药中的关键作用。这一发现为克服西妥昔单抗耐药提供了新的策略。
项目研究
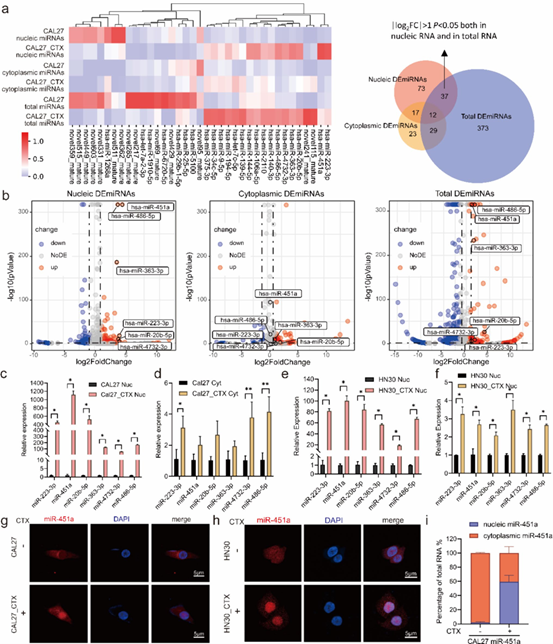
首先,作者检通过体外培养浓度递增的方法建立了西妥昔单抗耐药的细胞株。接下来,通过核质分离,分别对西妥昔单抗耐药和敏感细胞的细胞质、细胞核及全细胞裂解物进行小RNA测序。作者发现miR-451a在耐药细胞的细胞核中显著富集,且西妥昔单抗可以促进过表达miR-451a的核内富集,提示miR-451a可能与西妥昔单抗耐药相关。
Fig.1 miR-451a在西妥昔单抗耐药株中显著富集
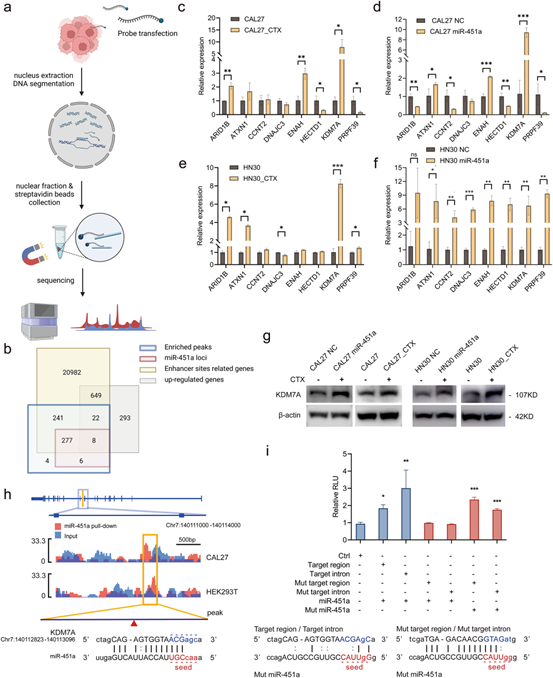
为探究miR-451a潜在的核内调控机制及靶点。作者通过体外转染miR-451a探针,并通过RNA纯化分离染色质并测序(ChIRP-seq),结合微阵列技术(microarray)及生物信息学分析,筛选miR-451a在西妥昔单抗耐药细胞株中的核内靶点。结果显示,位于KDM7A第10内含子上的增强子为核内miR-451a的靶点,其与miR-451a的相互作用促进KDM7A的表达。
Fig.2 miR-451a与KDM7A上的增强子区域相互作用并促进KDM7A表达
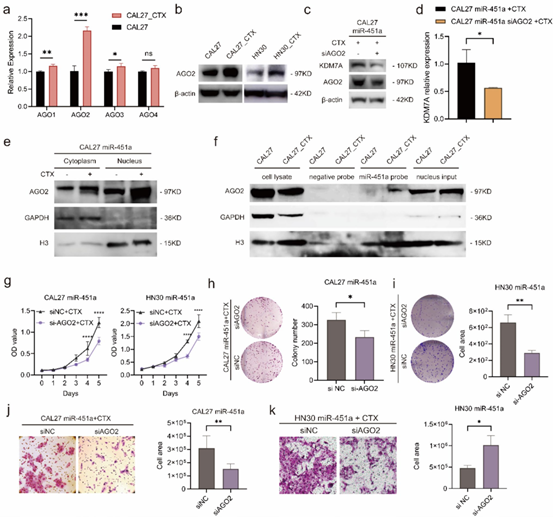
体外和体内的表型实验发现,miR-451a和KDM7A在西妥昔单抗刺激下促进肿瘤的增殖和迁移和移植瘤的生长。作者进一步分析了miRNA功能相关的重要媒介AGO蛋白的表达情况,发现AGO2在耐药株中表达上调。在西妥昔单抗刺激下,AGO2同样富集到细胞核内。RNA pull-down实验证明了miR-451a与AGO2在核内的相互作用。敲低ADO2的表达将抑制miR-451a对KDM7A的表达激活,也抑制了肿瘤细胞的增殖和迁移。
Fig.3 miR-451a通过AGO2依赖的方式促进KDM7A的表达
为了评估miR-451a及KDM7A在HNSCC西妥昔单抗治疗中的作用和潜在应用价值,作者收集了87例有西妥昔单抗治疗史的HNSCC患者样本,并检测了miR-451a和KDM7A在样本中的表达水平。q-PCR结果显示miR-451a和KDM7A在西妥昔单抗耐药患者中表达水平显著较高,且两者表达具有正相关性。miR-451a表达水平较高的患者生存期显著较低。对患者的临床病理资料分析发现miR-451a和KDM7A的高表达是西妥昔单抗耐药的显著风险因素,提示miR-451a和KDM7A可能可以作为西妥昔单抗预后的提示指标。
研究结论
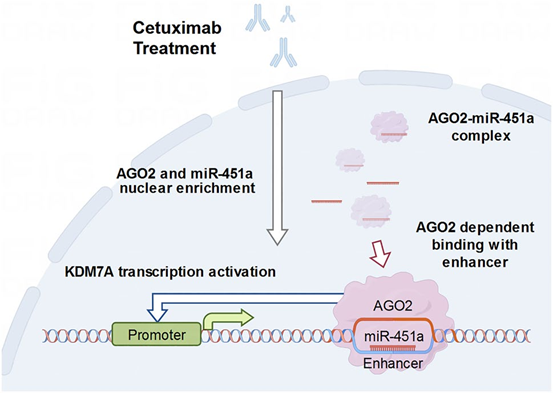
本研究揭示了miR-451a和AGO2介导的核激活途径在HNSCC西妥昔单抗耐药中的作用。
研究发现,西妥昔单抗促进miR-451a在细胞核中的富集,并通过靶向KDM7A内含子的增强子区域激活其表达。miR-451a和KDM7A是西妥昔单抗耐药的重要风险因素,有潜力作为耐药生物标志物或治疗靶点。这些结果为进一步研究RNA激活机制及改善肿瘤患者西妥昔单抗的耐药提供了依据。
吉满助力
本研究中所用的pGMR-TK报告基因质粒由吉满生物提供。 了解更多质粒构建,病毒包装,稳转株构建,敲除细胞株,报告基因检测等相关服务。欢迎访问吉满生物官网:www.genomeditech.com 免费咨询电话:400-627-9288 原文引用 “The Renilla luciferase reporter plasmid pGMR-TK was synthesized by Genomeditech (Shanghai, China).” 文献来源 https://link.springer.com/article/10.1007/s00018-024-05324-x 文章来源:课题组供稿