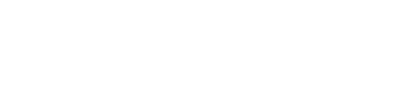靶点专栏
2026.05.14
GLP-1的热潮还未退去,代谢药物的下半场已经开始。相比“抑制食欲”,真正的下一步,是如何让身体“主动消耗能量”。本期我们聚焦这一新趋势下的潜力靶点布局--代谢轴(代谢与能量消耗)。
靶点一:FGF21
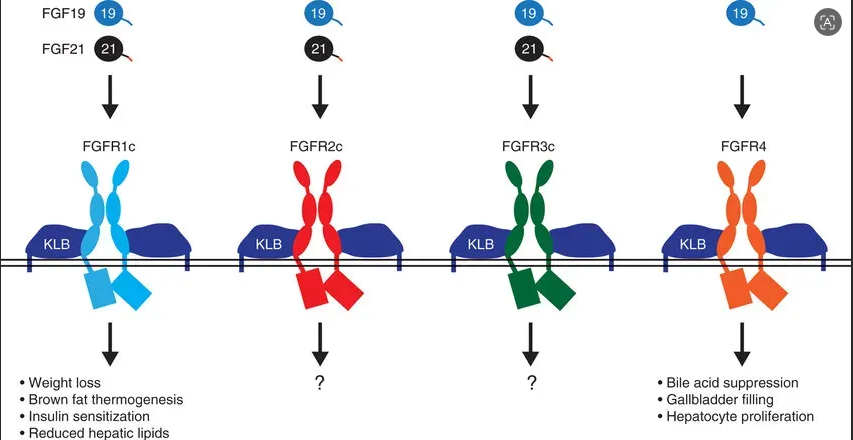
FGF21(成纤维细胞生长因子21)是一种由肝脏产生的代谢激素,通过由FGF受体1(FGFR1)和β-klotho组成的异二聚体受体复合体调节糖脂代谢,促进脂肪酸氧化、改善胰岛素敏感性,并降低肝脂沉积,因此被认为是连接肥胖、2型糖尿病及MASH的重要内分泌枢纽靶点。[1]
同时,在代谢疾病中普遍存在“FGF21抵抗”现象,即内源性FGF21升高但效应不足,为外源性FGF21替代或增强治疗提供了理论基础。
基于FGF21的多靶点策略正在兴起,FGF21/GLP-1双靶点及GLP-1R/GCGR/FGF21R三靶点激动剂,在降低肝脂、改善血糖及血脂方面显示出协同效应,进一步拓展了FGF21在代谢性疾病治疗中的应用前景。
FGF21在研药物进展
FGF21作为多通路代谢调控因子,在脂质代谢与胰岛素敏感性调节方面具有重要作用,其与GLP-1类药物在代谢改善机制上具有互补性,因此具有作为联合代谢干预靶点的开发潜力。
靶点二:THR-β
代谢功能障碍相关脂肪性肝炎(MASH)是一种与代谢紊乱相关的慢性肝脏疾病。改善MASH患者的代谢异常,主要包括改善胰岛素敏感性、减轻脂质积累、促进脂肪酸的氧化和消耗过程等,其中涉及的靶点就有THR-β。
甲状腺激素受体(THR)是一类重要的核受体蛋白,主要分为两类: α受体和β受体。
THRβ受体
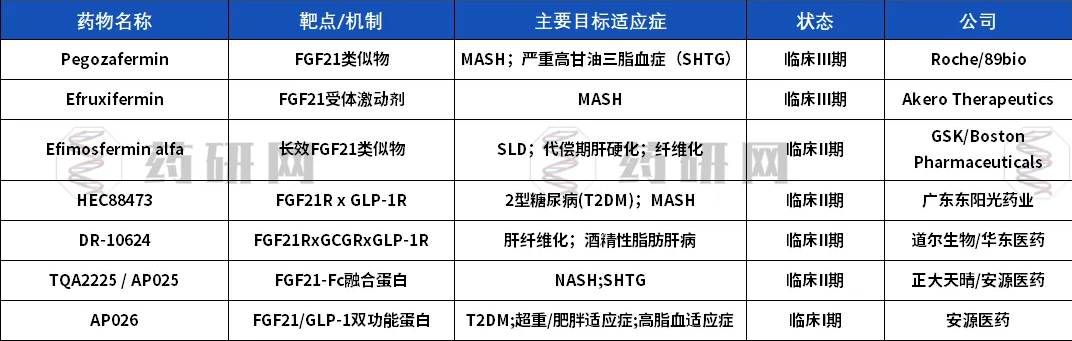
其中,THRβ是甲状腺激素发挥肝脏保护作用的主要亚型。THR-β作为一种核受体,其通路机制始于配体(如T3或激动剂)结合其配体结合域(LBD),诱导受体构象改变,使其从抑制状态(结合共抑制因子)转变为激活状态并招募共激活因子(如SRC-1),进而启动基因转录。
在肝脏代谢中,激活后的THR-β主要通过上调UCP1表达以增加产热和能量消耗,同时调节GLUT4表达以改善葡萄糖代谢和胰岛素敏感性,从而在发挥降低血脂、减少肝脏脂肪堆积等代谢益处时,能够避免由THR-α介导的心脏肥大等副作用。[3]
THRβ激动剂
THRβ激动剂已证实对肝脏具有多种有益作用,尤其是在治疗代谢功能障碍相关性脂肪肝(MASLD)和MASH方面。此外,THRβ激动剂还具有促进肝脏再生的潜力并可用于治疗其他疾病,例如肝细胞癌、动脉粥样硬化和中枢神经系统(CNS)疾病。

过去二十年来,人们致力于开发能够选择性地对肝脏产生有益作用并减少对心脏、肌肉和骨骼不良反应的THRβ激动剂。

THRβ激动剂药物[5]
靶点三:GPR75
全长G蛋白偶联受体75(GPR75)作为一种新兴的治疗靶点,因其在肥胖及代谢性疾病中的关键作用而备受瞩目。
表达系统
GPR75主要在中枢神经系统中表达,可被趋化因子CCL5/RANTES激活,进而与Gq蛋白偶联,触发肌醇三磷酸生成与钙离子动员,启动下游信号级联反应。
在下丘脑等关键脑区,GPR75通过调控与食欲相关的神经元活动,影响摄食行为与能量稳态,展现出显著的体重调节潜力。此外,GPR75可能与神经肽Y(NPY)、刺鼠相关肽(AGRP)及γ-氨基丁酸(GABA)共表达,形成协同调控网络,共同维持食欲与能量平衡。这一复杂的分子互作机制,进一步突显了GPR75在体重管理中的核心地位。
文献资料
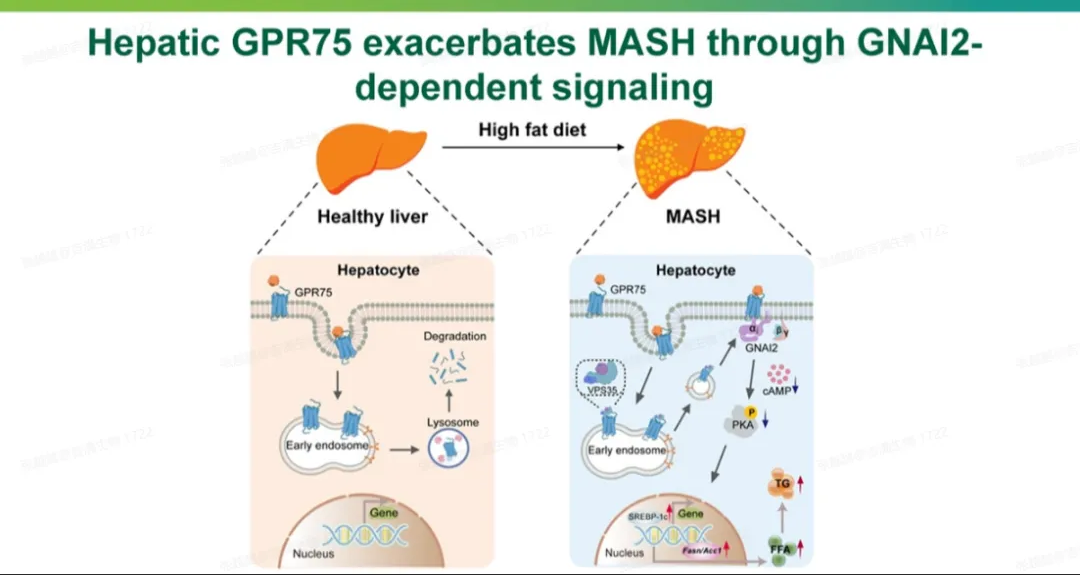
2026年2月,一项发表在肝病学期刊 《Hepatology》上的最新研究首次证实肝脏GPR75是MASH进展的关键驱动蛋白,且可作为治疗靶点。
研究证实GPR75经转录后调控在MASH中显著升高,通过GNAI2-cAMP-PKA通路驱动肝脂沉积、炎症与纤维化。这些发现表明,GPR75的抑制可能成为MASLD/MASH治疗的潜在治疗策略。[6]
在研进展
截至2026年3月,全球范围内尚无GPR75靶向药物进入临床阶段,整体仍处于早期探索期。其中Regeneron Pharmaceuticals与AstraZeneca合作推进小分子、siRNA及抗体等多技术路线开发,ConfometRx则仍处于先导化合物优化阶段。
国内方面,必贝特已披露首个GPR75间接抑制剂相关专利,并进入CMC开发阶段。
由于该赛道尚未出现First-in-class产品,且GPR75结构与作用机制的研究突破正在推动传统研发思路重构,也为具备早期技术积累的新兴Biotech提供了潜在的“卡位”机会。
靶点四:ASGR1
去唾液酸糖蛋白受体(ASGR,又称ASGPR)是一种C型凝集素受体,主要由主要亚基(ASGR1)和次要亚基(ASGR2)共同组成异源寡聚体复合物。
研究表明,去唾液酸糖蛋白受体在肝细胞表面和多种人类癌细胞系中高表达。作为在肝细胞表面高度富集且特异性极强的内吞受体,ASGR能够精准识别并结合带有末端半乳糖(Gal)或N-乙酰半乳糖胺(GalNAc)残基的多种配体,通过网格蛋白介导的内吞作用,将血液中衰老或去唾液酸化的糖蛋白内化并转运至溶酶体降解,从而在维持血清糖蛋白稳态中发挥核心作用。[7,8]
人类遗传学研究已经确定,ASGR1缺陷的变体与低胆固醇和心血管疾病的风险降低相关。
基于ASGR1独特的肝脏特异性表达与高效内吞特性,它已成为代谢性疾病领域备受瞩目的新型药物靶点。此外,还有一些研究表明靶向ASGR1可能存在治疗除降低血液胆固醇的其他肝脏疾病,例如肝硬化或慢性肝炎。

文献引用
近年来,宋保亮院士团队在《Nature》上发表的突破性研究发现,抑制ASGR1可激活LXR信号通路,上调ABCG5/G8转运蛋白的表达,从而促进胆固醇向胆汁排泄,大幅降低血液和肝脏中的脂质水平。这一发现不仅揭示了全新的降脂机制,也证实了ASGR1作为治疗高胆固醇血症靶点的巨大潜力。[10]
此外,ASGR1在肝脏病理生理过程中还扮演着“一因多效”的复杂角色。最新研究指出,ASGR1的缺失在发挥心血管保护作用的同时,可能会通过增加GP73介导的肝脏内质网应激,从而加剧肝损伤的风险。因此,深入探索靶向ASGR1的调控策略,不仅有望为高胆固醇血症提供全新的治疗手段,也对肝硬化、慢性肝炎等肝脏疾病的综合治疗具有重要的临床参考价值。
在研进展
ASGR1作为肝脏特异性靶点,目前有三款代表性在研药物进入不同研发阶段:AMG 529、SZN-043、SBT8230。三者均通过靶向ASGR1实现治疗目的,但作用机制与适应症存在显著差异,尚无药物推进至II期临床试验。
小 结
GLP-1的成功,推动代谢疾病治疗进入“系统调控”时代,而行业研发方向也正从“控制摄食”逐步转向“提升能量消耗”与“整体代谢改善”。
FGF21、THR-β、GPR75、ASGR1等靶点,分别从脂质代谢、能量消耗、中枢调控及肝脏稳态等维度切入,共同构建起下一代代谢治疗的新方向。随着多靶点联用与肝脏定向策略持续推进,代谢疾病治疗也正在从“减重”走向更全面的代谢干预。
吉满生物代谢类疾病的靶向药研发平台
肥胖和2型糖尿病(T2D)仍然是一个紧迫的全球健康危机。与此同时,多个与能量代谢、胰岛素分泌、食欲调控等作用机制紧密相关的靶点,在药物研发中同样扮演着关键角色,共同构成了这一领域的完整机制拼图。
合规基石与研发加速双驱动
吉满生物已成功获得HEK293、Jurkat E6.1、CHO-K1 等细胞商业使用授权,提供全面的溯源文件,赋能合作伙伴从临床前开发到IND/BLA 阶段进行合规研究,帮助客户规避法律风险并加速商业化进程。

全靶点覆盖的精准工具体系
吉满生物专注于FGF21/THR-β/GPR75/ASGR1靶点研发,现提供相关稳定表达细胞系、报告基因细胞系、抗体、蛋白等产品,覆盖代谢疾病领域从药物筛选到作用机制研究的关键环节。助力药企加速MASH、糖尿病等方向创新药研发与临床申报进程。(详情咨询吉满客服:18916119826)
产品清单

数据展示(部分)
GM-C19834:H_FGF21 Reporter HEK-293 Cell Line
该细胞产品传代至少28代后,信号响应仍然稳定

使用Recombinant Human FGF-21 Protein
稳定性验证结果
GM-C30364:H_THRβ Reporter HEK-293 Cell Line
经 Liothyronine sodium (T3) 严格的功能实测,结果显示细胞对激素响应准确、信号传导通畅,高效助力药物筛选与活性评价。

使用Liothyronine sodium验证结果
GM-C21636:H_GPR75 HEK-293 Cell Line
经抗体验证,该细胞系产品表达稳定
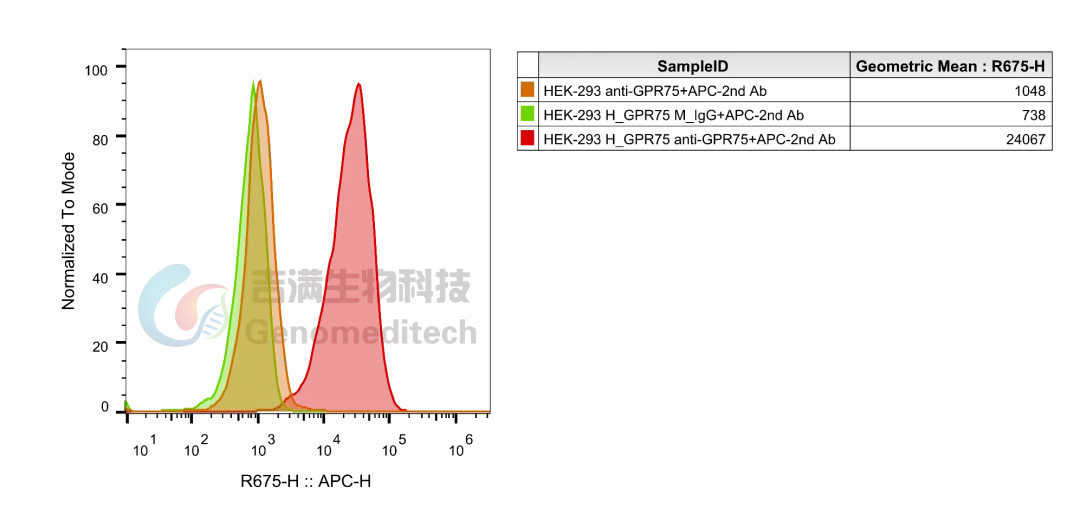
使用Human GPR75 Antibody验证结果
GM-C41613:H_ASGR1 HEK-293 Cell Line
该细胞产品传代至少30代后,表达仍然稳定
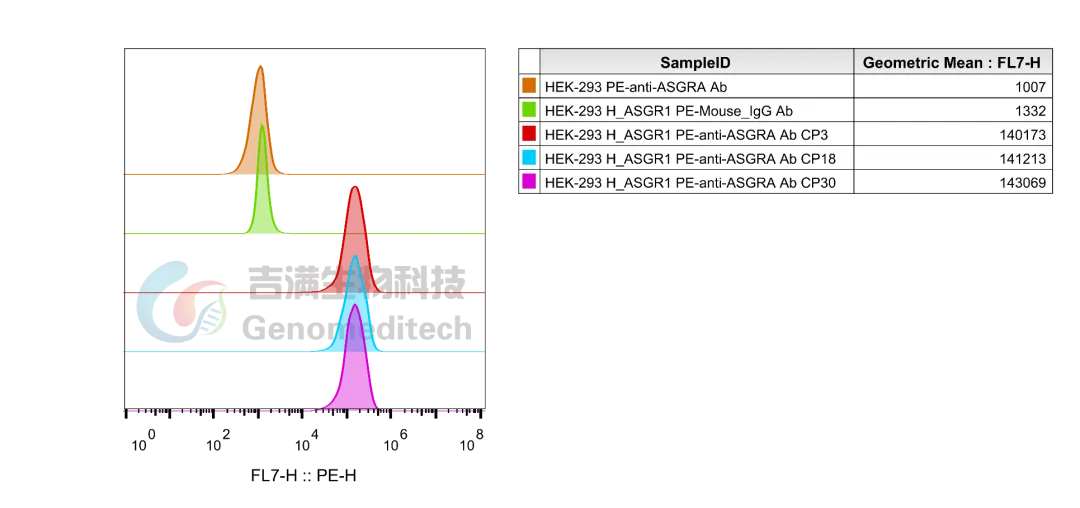
使用Anti-ASGR1 Antibody稳定性验证结果
联系我们
吉满生物专注为生物药开发,提供高效的研发工具和解决方案。截止当前已布局近400个热门靶向药靶点,超1500株现货单克隆细胞系,涵盖肿瘤相关抗原(TAA)、 免疫检查点、Fc受体、细胞因子和激酶等热门靶点类型。旨在助力、加速大分子早期研发,做到进口细胞的国产替代。
参考文献:
[1] Shao W, Jin T. Hepatic hormone FGF21 and its analogues in clinical trials. Chronic Dis Transl Med. 2022 Feb 23;8(1):19-25. doi: 10.1016/j.cdtm.2021.08.005. PMID: 35620160; PMCID: PMC9126297.
[2] Geng L, Lam KSL, Xu A. The therapeutic potential of FGF21 in metabolic diseases: from bench to clinic. Nat Rev Endocrinol. 2020 Nov;16(11):654-667. doi: 10.1038/s41574-020-0386-0. Epub 2020 Aug 6. PMID: 32764725.
[3] https://doi.org/10.1016/j.apsb.2024.07.025
[4] https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
[5] https://www.madrigalpharma.com/therapeutic-focus/[6] Yang X, Yang N, Cheng
[6] Zhang R, Fan H, Liu D, Aa J, Wang G, Xie Y. Hepatic GPR75 exacerbates MASH through GNAI2-dependent signaling. Hepatology. 2026 Feb 3. doi: 10.1097/HEP.0000000000001706. Epub ahead of print. PMID: 41632920.
[7] https://en.wikipedia.org/wiki/Asialoglycoprotein_receptor
[8] https://www.proteinatlas.org/ENSG00000141505-ASGR1/cancer
[9] https://doi.org/10.1371/journal.pgen.1009891.g007
[10] Wang, JQ., Li, LL., Hu, A. et al. Inhibition of ASGR1 decreases lipid levels by promoting cholesterol excretion. Nature 608, 413–420 (2022). https://doi.org/10.1038/s41586-022-05006-3