文献解读
西安交通大学第一附属医院吴岳教授团队在《Blood》在线发表题为“Targeting FXR in Hepatocytes: A Promising Approach to Enhance Fibrinolysis and Reduce Deep Vein Thrombosis Risk”的文章。
该研究提出,营养感应核受体FXR可负向调控肝细胞PAI-1表达,FXR失活可能导致纤溶受损并促进血栓形成,为肥胖相关DVT防治提供新的分子靶点。
研究背景
肥胖是一项全球性的重大健康挑战,也是静脉血栓栓塞性疾病(VTE)的危险因素。纤溶酶原激活物抑制剂1(PAI-1,由基因SERPINE1编码)是纤溶的负调控因子,长期被认为与深静脉血栓(DVT)密切相关。
过去认为脂肪细胞是PAI-1主要来源,但研究表明约70%的血浆PAI-1由肝细胞产生,肝脏在肥胖相关纤溶障碍中起核心作用。然而,肥胖导致PAI-1表达变化的分子机制仍未被明确。
项目研究
高脂饮食(HFD)小鼠表现出纤溶时间缩短和深静脉血栓(DVT)负担加重的特征
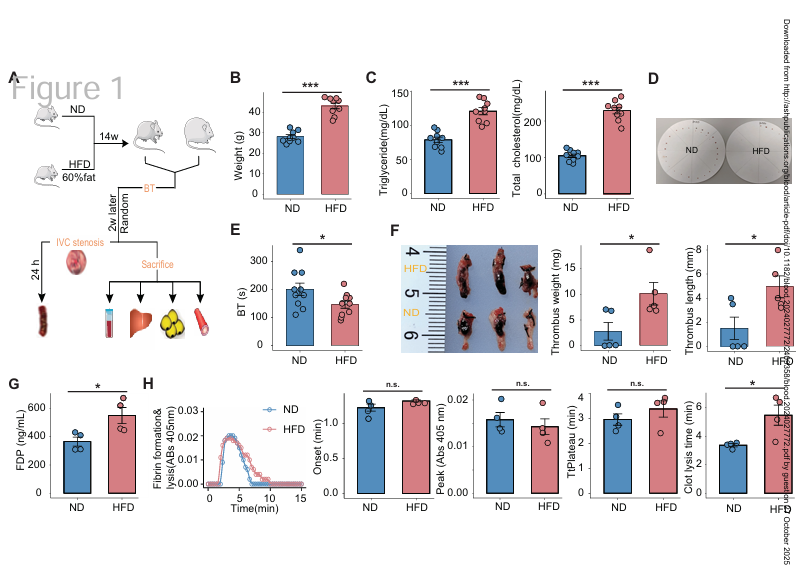
为评估高脂饮食(HFD)对血栓相关表型的影响,作者对连续喂养高脂饮食或正常饮食(ND)16周的雄性C57BL/6J小鼠进行了血液学及代谢指标检测。
与ND小鼠相比,HFD小鼠体重及血浆甘油三酯、胆固醇显著升高;同时血栓负荷增加。重要的是,HFD小鼠血浆纤维蛋白降解产物(FDP)升高,表明体内纤维蛋白形成与溶解过程被激活。
功能检测显示,HFD小鼠血浆纤维蛋白形成动力学基本正常,但凝块溶解时间显著延长,表明纤溶能力下降。这些结果提示高脂饮食导致DVT负担增加,部分原因是纤溶反应能力下降。
Fig.1 高脂饮食(HFD)可延缓小鼠的纤溶过程并
加重深静脉血栓(DVT)负担
肝脏PAI-1过度表达介导了肥胖所致的纤溶功能障碍
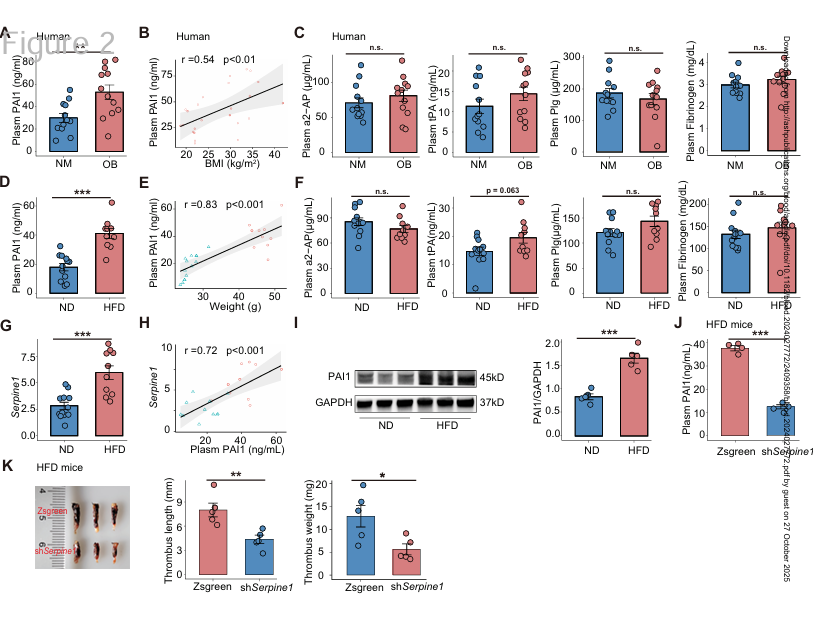
为探究肥胖状态下纤溶活性降低的分子机制,研究首先检测了已知会影响纤溶系统的循环成分。结果显示,肥胖人群与高脂饮食小鼠的血浆 PAI-1显著升高并与体质指数(BMI)正相关;
进一步研究发现血浆PAI-1的主要来源为肝脏,并过向HFD小鼠注射了肝脏特异性AAV8-TBG-shSerpine1,并诱导下腔静脉狭窄。该干预显著降低了血浆PAI-1水平,同时减小了血栓的长度和重量。因此,肥胖导致肝脏PAI-1表达上调,从而引起血浆纤溶功能受损。
Fig.2 肥胖可提高小鼠肝脏及循环系统中的PAI-1水平
转录组学和靶向胆汁酸代谢组学分析表明,肥胖导致FXR信号通路异常
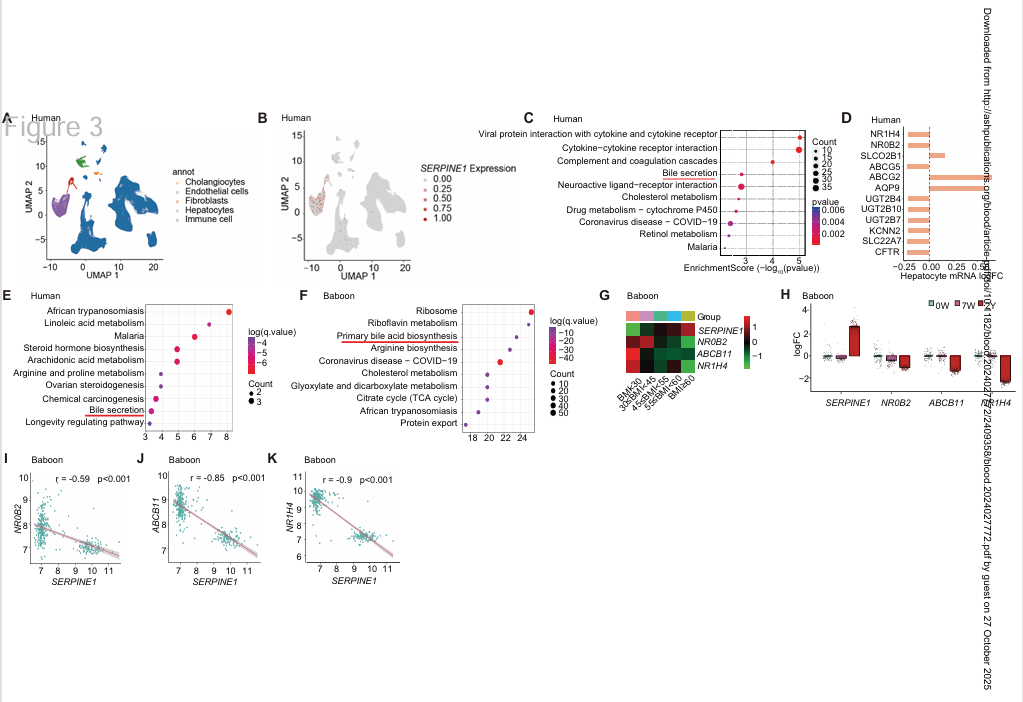
转录组学与靶向胆汁酸代谢组学分析表明,肥胖会导致肝脏FXR信号通路受损,从而促进PAI-1(Serpine1)过度表达。
单细胞RNA测序数据显示,Serpine1主要在肝细胞中高表达;差异基因富集分析揭示,肥胖者肝脏中胆汁酸分泌通路显著富集,其相关基因多为FXR的直接或间接靶基因。在肥胖人群、长期高脂饮食(HFD)狒狒及小鼠肝脏中,FXR(NR1H4)及其靶基因ABCB11和NR0B2表达普遍下降,与SERPINE1呈显著负相关,提示FXR信号受抑是PAI-1上调的重要原因。
体外实验进一步证实,棕榈酸处理小鼠原代肝细胞后,Serpine1转录与PAI-1分泌明显增加,而FXR及其靶基因Nr0b2、Abcb11显著下调,呈负相关关系。综合结果表明,肥胖通过抑制肝细胞FXR信号通路,诱导PAI-1过度表达和分泌,从而削弱纤溶功能并促进血栓形成。
Fig.3 肥胖状态下PAI-1上游调控因子的预测
FXR缺失小鼠表现出纤溶功能受损和加重的深静脉血栓(DVT)负担
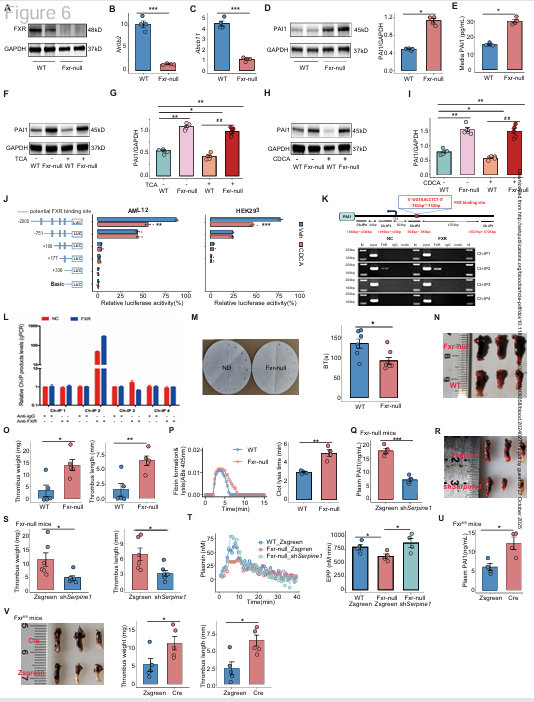
双荧光素酶及ChIP实验显示,FXR通过结合PAI-1启动子−761至−752 bp区域抑制其转录。也就是说,FXR直接负向调控PAI-1基因表达,从而降低肝细胞及循环系统中PAI-1水平。
为直接评估FXR缺失对血浆纤溶功能及DVT的影响,研究构建了FXR基因敲除(Fxr-null)小鼠,其肝脏及血浆中PAI-1 mRNA和蛋白水平均显著升高,并表现出出血时间缩短、血栓长度和重量增加、凝块溶解时间延长等特征,而纤维蛋白形成无变化,提示纤溶功能受损而非凝血增强。
为验证PAI-1的作用,研究利用肝靶向AAV-TBG-shSerpine1沉默Serpine1,结果血浆PAI-1下降,血栓负担显著减轻,内源性纤溶潜能(EPP)及峰值恢复至正常水平,证明PAI-1在FXR缺失致纤溶障碍中起关键作用。总之,FXR缺失导致PAI-1过度表达、纤溶受损,从而加重血栓形成,揭示FXR–PAI-1通路在血栓调控中的核心作用。
Fig.4 FXR在调控PAI-1表达中的作用及其对血浆纤溶功能和深静脉血栓(DVT)的影响
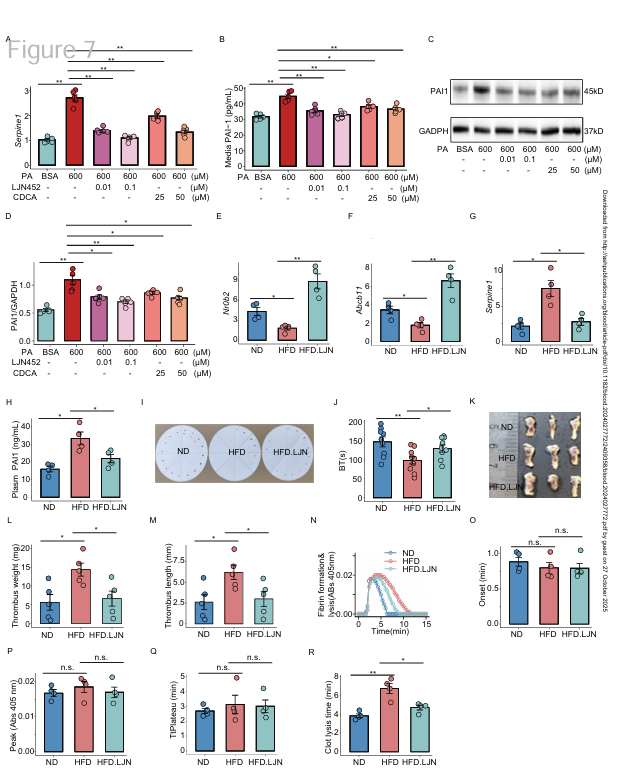
FXR激动剂tropifexor可显著改善高脂饮食(HFD)诱导的小鼠纤溶活性下降和深静脉血栓(DVT)负担加重的病理状态
在体外实验中,为模拟肥胖引起的低纤溶活性,小鼠原代肝细胞(MPHs)经棕榈酸处理后,再分别与FXR激动剂GW4064、CDCA或tropifexor共同孵育。
结果显示,这些FXR激动剂均能显著降低细胞内及培养上清中的PAI-1蛋白和mRNA水平。在体内实验中,经tropifexor处理的HFD小鼠肝脏中FXR表达略有上调,肝脏Serpine1和血浆PAI-1表达显著下降。
功能性检测显示,tropifexor处理组HFD小鼠出血时间延长,纤维蛋白形成与溶解过程加快,血栓重量与长度均明显减小,提示药物有效改善了肥胖相关的纤溶障碍与血栓负担。
Fig.5 FXR激动剂可改善肥胖导致的纤溶功能受损并减轻深静脉血栓(DVT)负担
研究结论
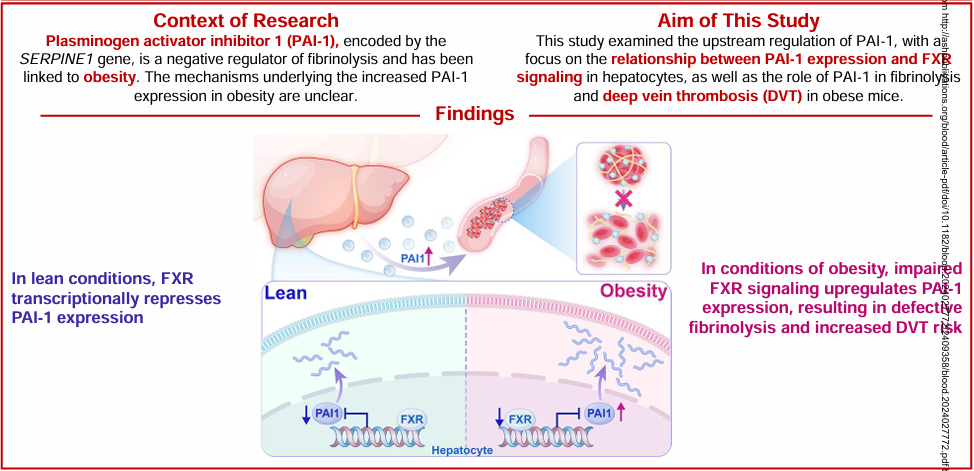
本研究发现,靶向激活肝细胞FXR信号可显著抑制PAI-1表达,从而增强肥胖小鼠的纤溶活性并减轻DVT负担。通过强制性调控FXR不仅有效降低血浆PAI-1水平,还能改善纤溶相关代谢特征,最终减少血栓形成,说明FXR对PAI-1的调节在纤溶和DVT的发生发展中具有关键作用。为以“肝细胞FXR—PAI‑1轴”为靶点的抗血栓治疗提供了理论依据。
在正常状态下,FXR通过转录抑制方式降低PAI-1的表达;而在肥胖状态下,受损的FXR信号传导会上调PAI-1的表达,导致纤溶功能障碍并增加深静脉血栓(DVT)风险。
吉满生物
如想了解更多质粒构建、病毒包装、稳转株构建、敲除细胞株、报告基因检测等相关服务。欢迎访问吉满生物官网:www.genomeditech.com
免费咨询电话:400-627-9288
文章DOI: 10.1182/blood.2024027772