靶点专栏
靶向PD-1/PD-L1轴的免疫检查点抑制剂通过恢复耗竭的细胞毒性T细胞的功能,重塑了癌症免疫疗法。
PD-1/PD-L1
PD-1/PD-L1 抑制剂通过阻断 PD-1 与其配体 PD-L1 之间的相互作用,能够恢复耗竭的细胞毒性 T 细胞(CTL)功能,从而在多种肿瘤治疗中取得突破性进展。然而,单独应用 PD-1/PD-L1 抑制剂的疗效仍受限制,部分肿瘤表现出原发性或继发性耐药,这主要与肿瘤微环境中 T 细胞的浸润、扩增及活化受限有关。
为了克服这一局限性,细胞因子工程,特别是通过调节白细胞介素-2 (IL-2) 通路,已成为一种重要的补充策略。
IL-2
IL-2是调节T细胞增殖、存活和功能的关键因子,其信号主要通过高亲和力受体 IL-2Rαβγ(CD25/CD122/CD132)传导。传统高剂量IL-2治疗虽然可以激活效应T细胞,但同时也会过度激活调节性T细胞(Treg),导致抗肿瘤免疫受抑制,并伴随严重全身毒性,例如毛细血管渗漏综合征(CLS)。
为解决这些问题,IL-2 变体(IL-2v)被设计以调控 IL-2 与 CD25 的结合亲和力,从而选择性激活抗肿瘤T细胞,同时降低副作用。[1]
研发进展
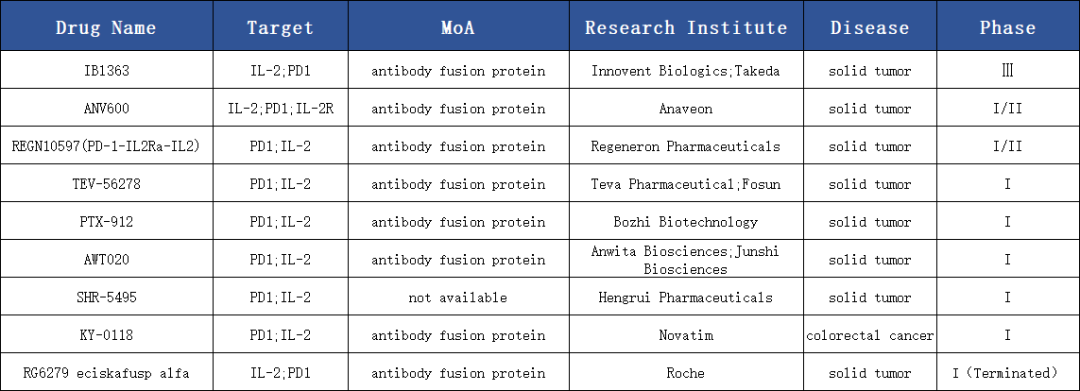
PD-1/IL-2研发进展较快的药物格局
在 PD-1 × IL-2v 融合免疫疗法领域,罗氏(Roche)与信达生物(Innovent)提出了截然不同的分子设计理念。
罗氏PD-1×IL-2 融合蛋白 RG6279
采用 βγ-biased IL-2v,即完全去除 IL-2 与 α 受体(CD25)的结合能力,保留 βγ 受体的天然亲和力,其通过 PD-1 抗体顺式靶向(cis-targeting)将 IL-2v 递送至 PD-1⁺ T 细胞,以期绕开 CD25 依赖、促进干细胞样 CD8⁺ T 细胞(Tpex)激活。
信达IBI363
采取α-biased IL-2v 策略,保留 IL-2 与 CD25 的高亲和结合,同时显著削弱βγ结合活性。IBI363 通过降低整体 IL-2 活性,使分子可在 3 mg/kg 高剂量下安全递送,达到 PD-1 抗体的有效治疗水平,同时在肿瘤内恢复高 IL-2 活性,实现强效抗肿瘤反应。[2]
2025 年 10 月,信达与武田制药达成全球战略合作,武田获得 IBI363 在大中华区以外的全球权益。这一合作被业内视为近年来免疫肿瘤学领域最重要的授权交易之一。IBI363 目前正用于评估非小细胞肺癌(NSCLC)和微卫星稳定型结直肠癌(MSS CRC)的治疗效果。[4]
小 结
PD-1–IL-2v 融合免疫疗法的出现,标志着肿瘤免疫治疗正从单一检查点阻断迈向多维度的免疫调控阶段。
通过将检查点靶向与细胞因子工程相结合,研究者能够在空间和受体层面上实现对免疫效应细胞的精准激活。然而,如何在提升疗效的同时保持安全性,仍是该领域亟待解决的核心问题。
用心做好细胞,为更好的靶向药
此类双功能融合生物制剂的评估需要能够准确反映PD-1结合和IL-2R信号传导的体外系统。
在此背景下,吉满生物精准开发了GM-C41979 / H_CD25 CD122 CD132 Reporter Jurkat (hPD1 OE) Cell Line 报告基因细胞系产品,助力PD-1–IL-2v 新型免疫治疗药物研发。此处点击了解PD-1/IL-2相关产品
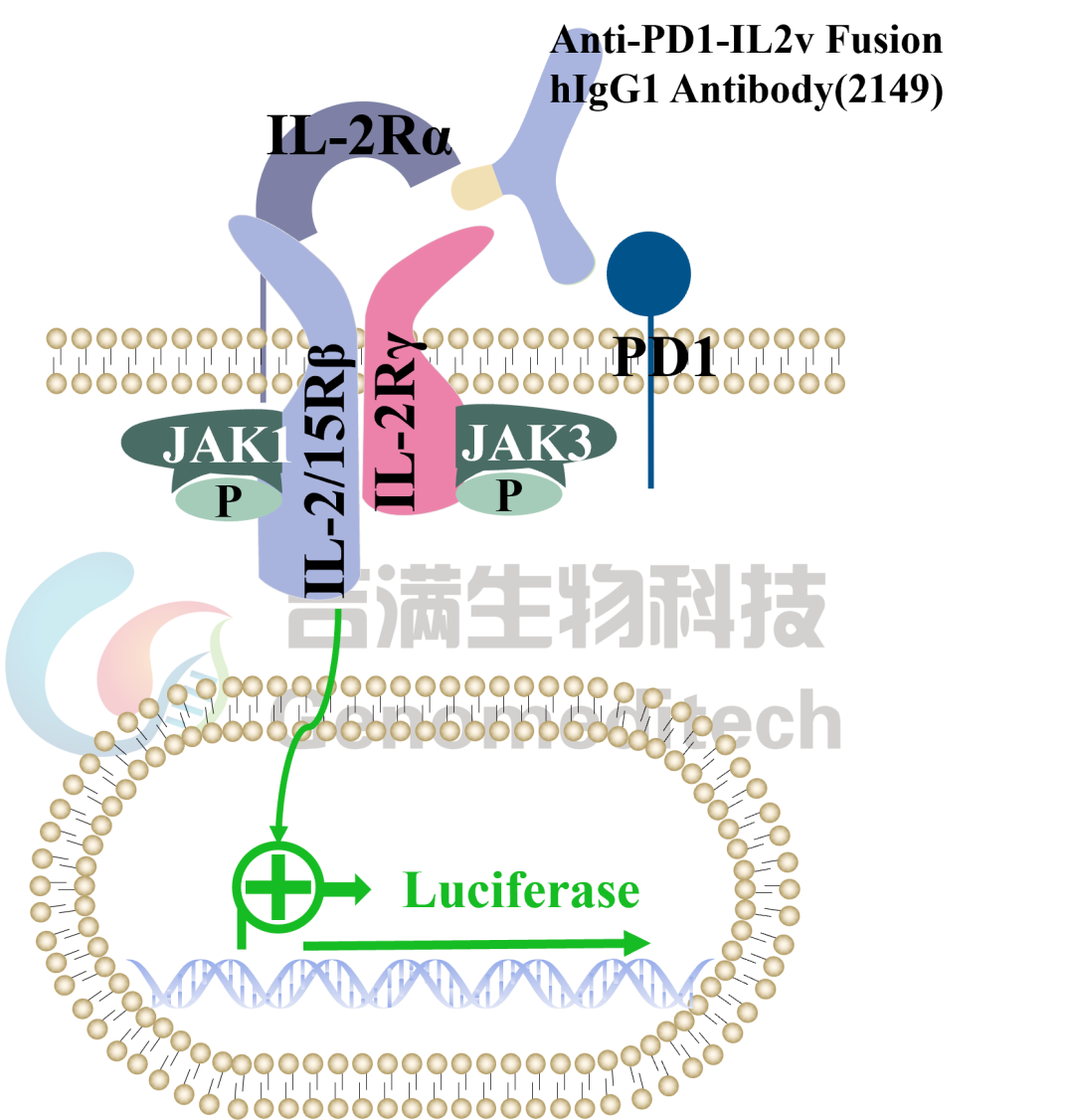
该细胞系基于 Jurkat T 细胞,利用慢病毒技术实现稳定克隆化表达 CD25(IL‑2Rα)、CD122(IL‑2Rβ)、CD132(IL‑2Rγ) 以及 PD‑1 分子,并导入 信号依赖型荧光素酶报告基因。
当 抗 PD‑1–IL‑2v 融合抗体 结合 PD‑1 并递送 IL‑2v 至受体复合物后,IL‑2R 下游信号被激活,诱导荧光素酶表达。荧光读数与信号强度正相关,从而定量反映融合抗体的生物活性。
应用场景
PD‑1–IL‑2v 融合疗法通过将细胞因子递送限制于 PD‑1 高表达 T 细胞,实现空间精准的免疫激活。
该产品借助其双受体(PD‑1 与 IL‑2R)设计,能够:
定量测量不同药物浓度下 PD‑1 依赖性 IL‑2R 信号强度
比较不同构型 PD‑1–IL‑2v 分子的效力与EC₅₀差异
区分 PD‑1 依赖性与非依赖性细胞因子效应
在药物优化与质量控制阶段提供快速、可重复的体外检测平台
功能验证与特异性确认
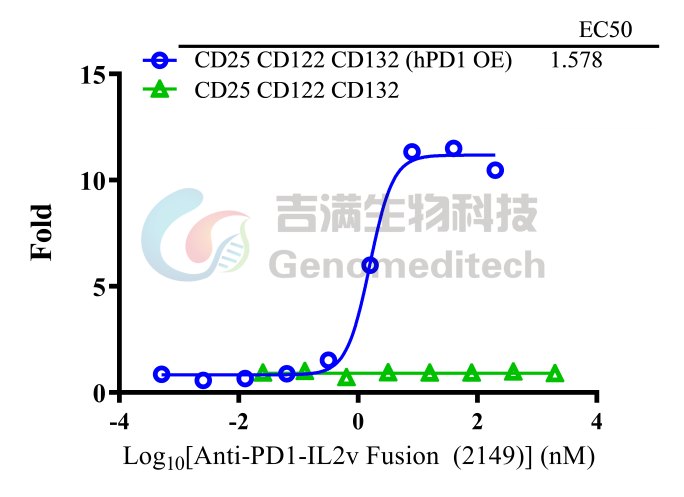
在相同检测条件下对 GM‑C41979 与其 PD‑1 阴性亲本对照系(H_CD25 CD122 CD132 报告基因 Jurkat,GM‑C29055) 进行比较。
验证结果显示:吉满生物GM‑C41979 报告基因细胞系产品能特异、可重复地反映 PD‑1 依赖的 IL‑2R 信号通路,是 PD‑1–IL‑2v 类药物体外活性验证的理想模型。
重组抗 PD1-IL2v 融合 hIgG1 抗体 (2149) 的比较反应
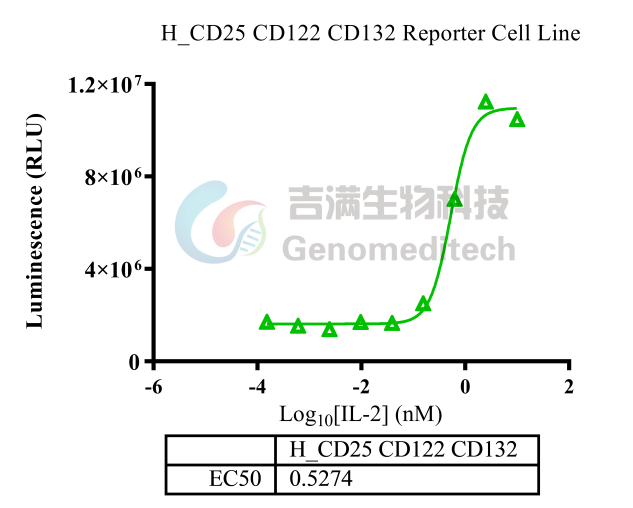
对重组人IL- 2的反应
非 PD-1 表达 IL-2 报告细胞中的反应比较
受体表达验证
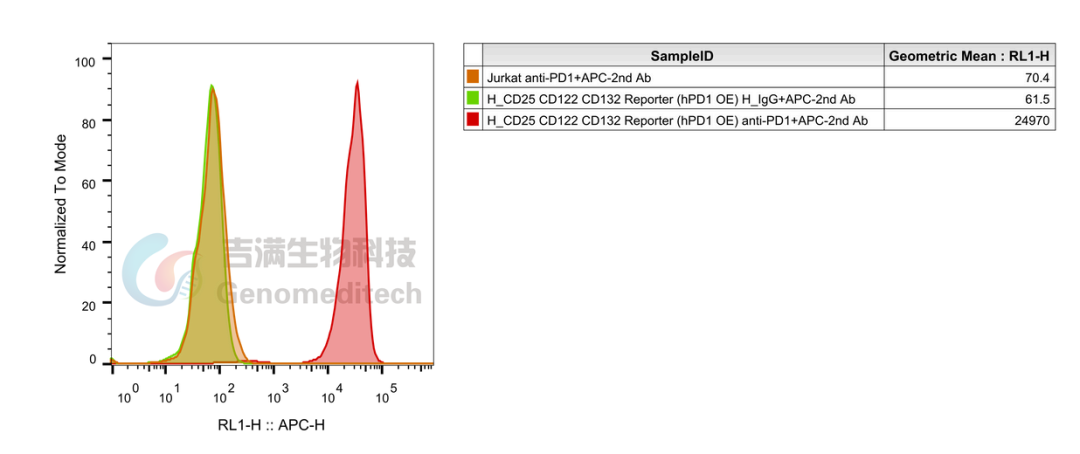
通过流式细胞术,使用了四种抗体分别验证了 PD‑1 及三种 IL‑2 受体亚基的表达。
检测结果显示:GM‑C41979 细胞均为阳性,说明目标分子表达稳定、结构完整。
流式细胞术证实PD-1表达
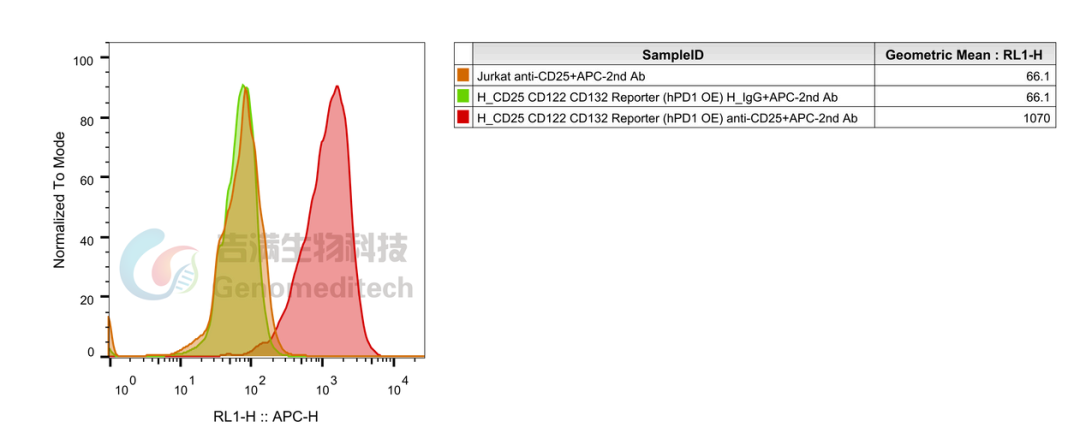
流式细胞术证实IL-2Rα(CD25)表达
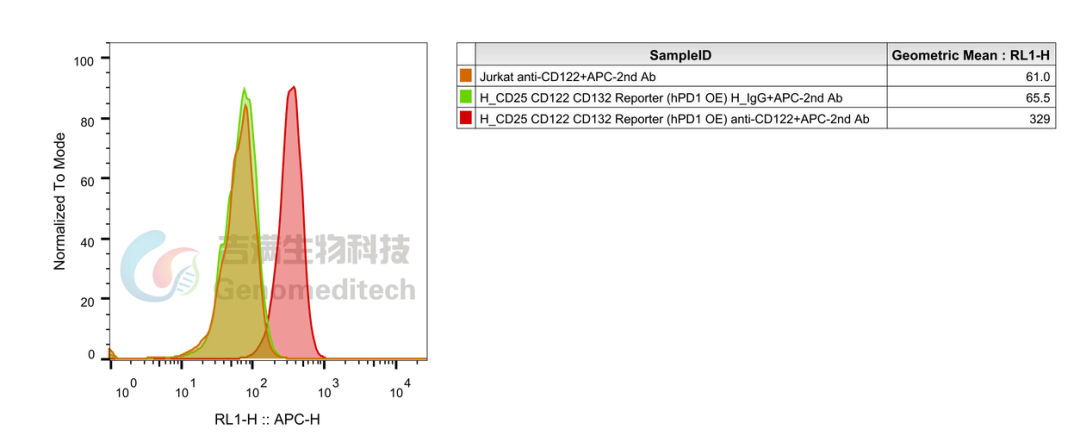
流式细胞术证实IL-2Rβ(CD122)表达
流式细胞术证实IL-2Rγ(CD132)表达
联系我们
吉满生物专注为生物药开发,提供高效的研发工具和解决方案。截止当前已布局近400个热门靶向药靶点,超1000株现货单克隆细胞系,涵盖肿瘤相关抗原(TAA)、 免疫检查点、Fc受体、细胞因子和激酶等热门靶点类型。旨在助力、加速大分子早期研发,做到进口细胞的国产替代。同时构建了丰富的蛋白、抗体及试剂现货产品库。
参考资料
[1] DOI=10.3389/fimmu.2023.1218082
[2] https://www.prnewswire.com/news-releases/2025-asco-oral-presentation-innovent-biologics-announces-updated-date-of-ibi363-first-in-class-pd-1il-2-bias-bispecific-antibody-fusion-protein-from-phase-1-clinical-studies-in-advanced-colorectal-cancer-302470217.html
[3] https://www.roche.com/investors/events/hy-2025
[4]https://www.takeda.com/newsroom/newsreleases/2025/innovent/
[5] https://www.guidechem.com/guideview/phar/roche-terminates-tigit-trials-updates-pipeline.html