研究背景
三阴性乳腺癌(Triple-negative breast cancer,TNBC)是乳腺癌的一种亚型,表现为对雌激素受体、孕激素受体和HER2蛋白的阴性。
在所有乳腺癌中,TNBC以其高侵袭性和不良预后而著称。转移是导致TNBC高死亡率的重要因素,理解其分子机制至关重要。
文献来源
2024年10月,《Molecular Cancer》期刊发表了题为“Tumor-intrinsic role of ICAM-1 in driving metastatic progression of triple-negative breast cancer through direct interaction with EGFR”的研究论文。
在该研究中,作者发现细胞间黏附分子ICAM-1在转移性乳腺癌中的表达水平升高,并且作为表皮生长因子受体(EGFR)激活的关键结合适配器,对恶性肿瘤进展起着至关重要的作用。
项目研究
研究团队通过GEO数据库分析筛选到了在TNBC中高特异性表达的靶标 ICAM-1,并展开研究其临床意义与潜在机制。
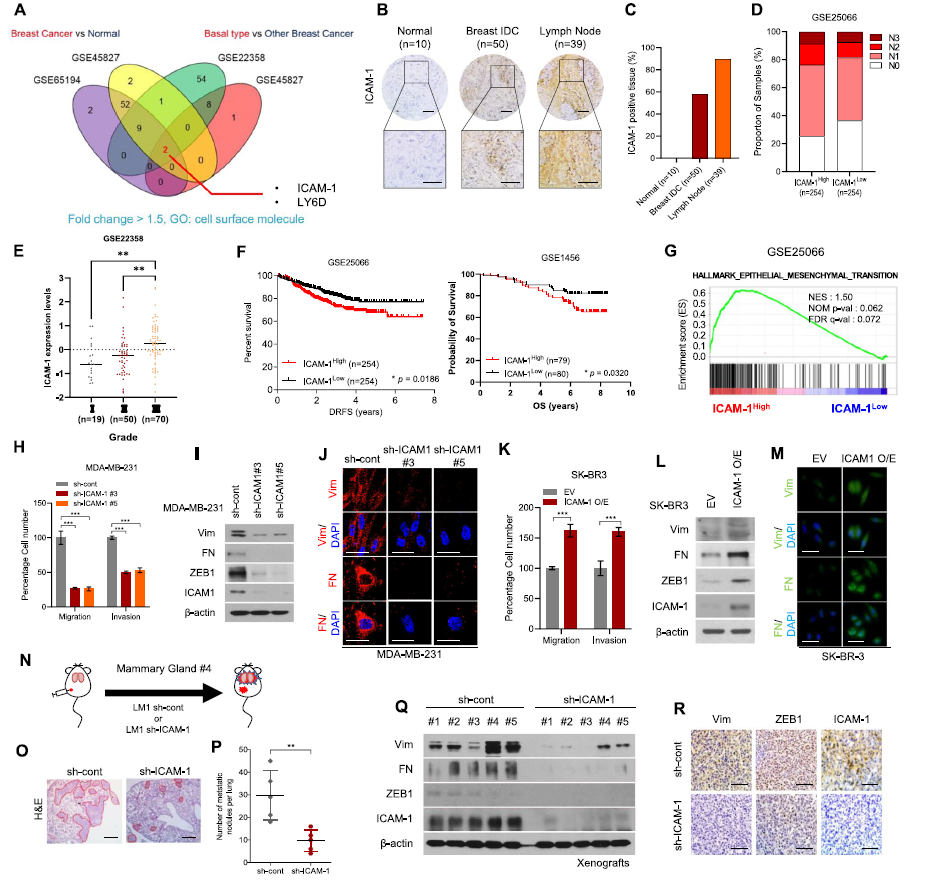
临床数据显示,高ICAM-1表达水平与乳腺癌患者的低总生存率显著相关。之后验证了ICAM-1在三阴性乳腺癌(TNBC)中的功能及机制,ICAM-1通过shRNA或者敲除抑制了乳腺癌细胞的迁移和侵袭,EMT标志物和调节因子表达变低,过表达ICAM-1与之相反。同样,在LM 1 sh-ICAM-1荷瘤小鼠中,原发性肿瘤的肺组织肿瘤转移和EMT标记物表达降低。体内外研究均表明ICAM-1介导的EMT促进乳腺癌细胞的转移。
Fig.1 ICAM-1的上调与乳腺癌的不良预后和转移相关
为了了解ICAM-1如何促进乳腺癌转移,作者分离并验证了与ICAM-1相互作用的蛋白质-EGFR。
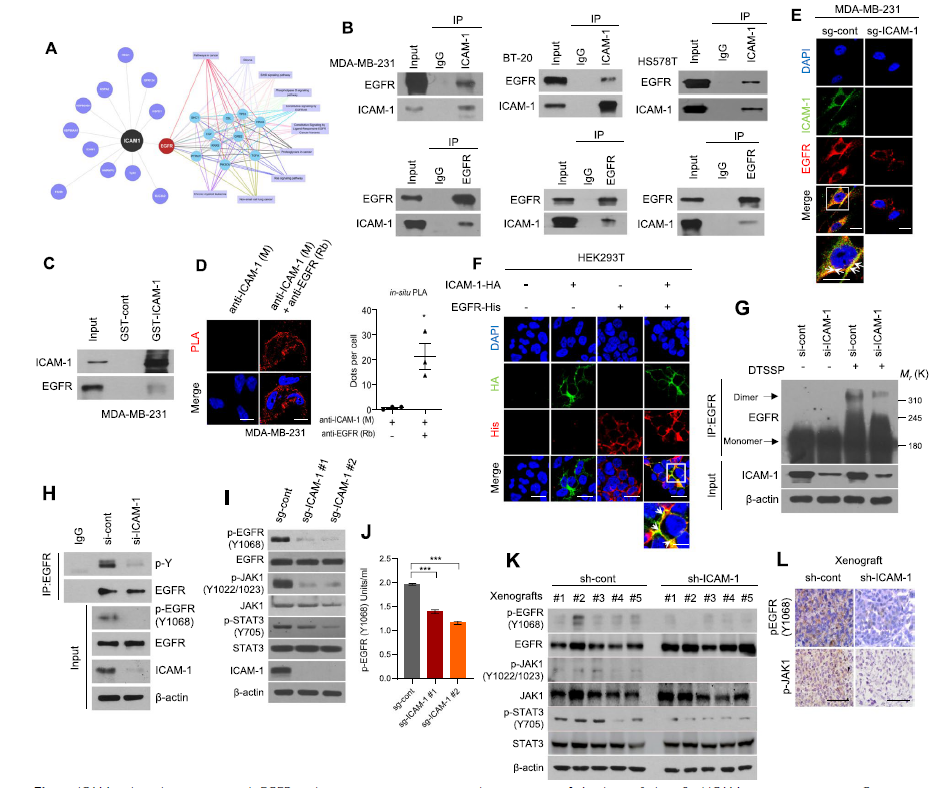
敲低ICAM-1抑制EGFR活性(如EGFR、JAK 1和STAT 3磷酸化和EGFR二聚化增加),但不改变EGFR的总蛋白水平。在携带LM 1 shICAM-1肿瘤的小鼠中观察到了相似的结果。相反,ICAM-1过表达增强了EGFR活性。也就是说,ICAM-1和EGFR直接相互作用增加了EGFR活性和下游信号通路。
Fig.2 ICAM-1和EGFR之间的直接相互作用增加了EGFR的活性和下游信号传导
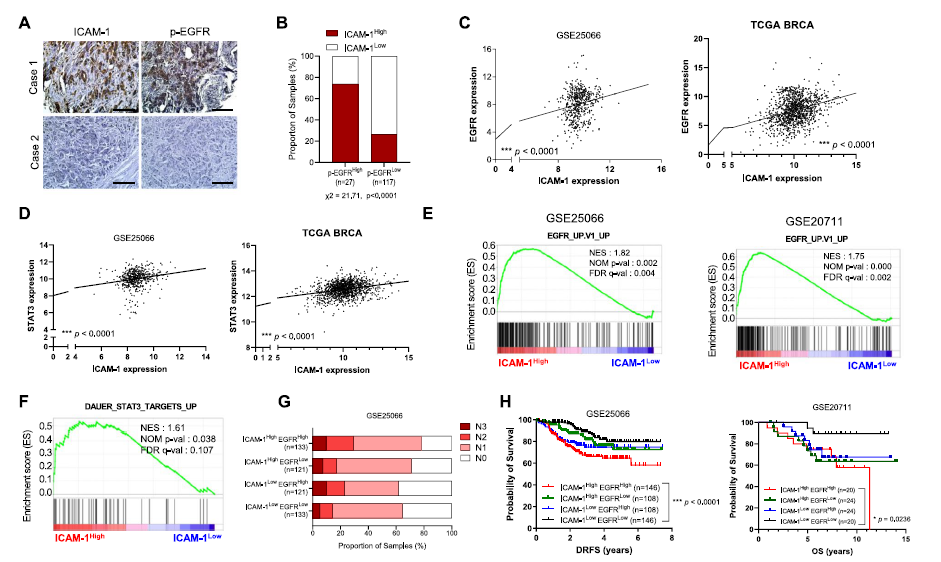
接下来研究了乳腺癌患者中 ICAM-1 与EGFR 活化之间的相关性。通过数据集发现ICAM-1 表达与 EGFR 、 STAT3 表达呈正相关;综合临床数据表明,高水平的 ICAM-1 表达与乳腺癌患者的 EGFR 表达以及不良预后相关。
Fig.3 高水平的 ICAM-1 表达与乳腺癌患者的 EGFR 表达和不良预后相关
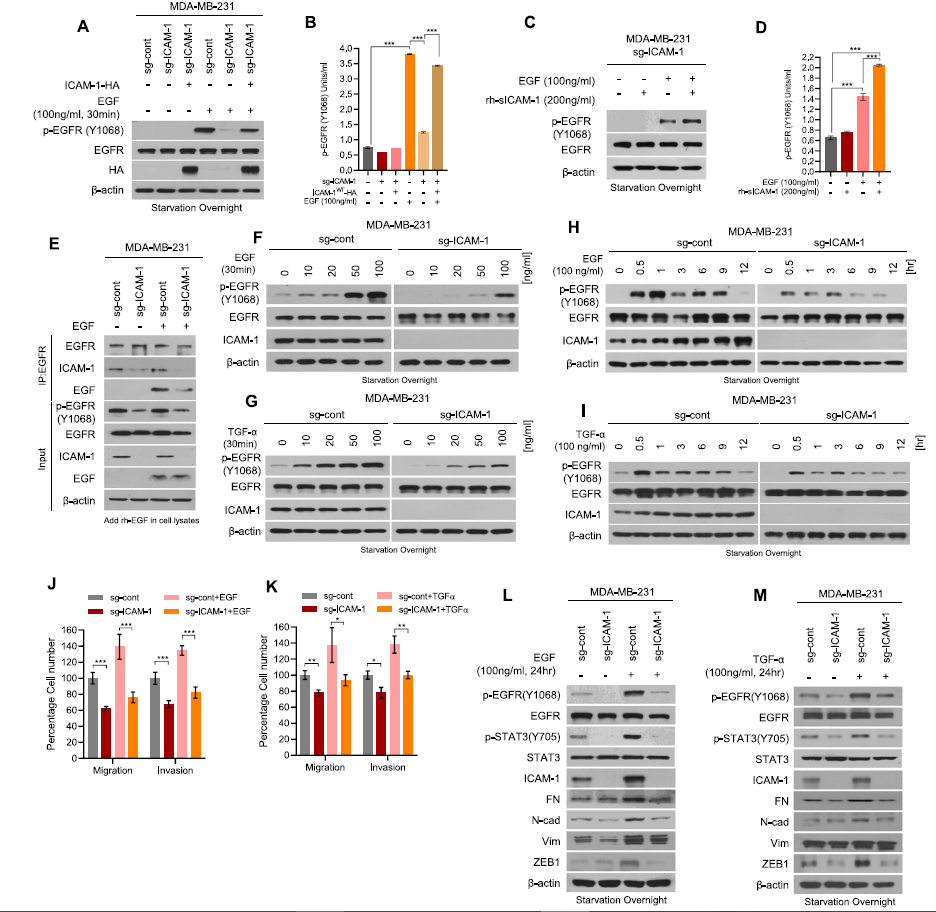
随后,作者进一步通过体内及体外实验证明了 ICAM-1 表达与 EGFR 活化之间的联系,以及它对乳腺癌患者临床结果的影响;通过敲除和过表达ICAM-1 基因,做了一系列WB,COIP等实验表明了ICAM-1 增加 EGFR 的配体结合亲和力并促进乳腺癌的转移。
Fig.4 ICAM-1 增加 EGFR 的配体结合亲和力并促进乳腺癌的转移
随后,作者使用蛋白质-蛋白质对接模拟研究了 ICAM-1 和 EGFR 之间的相互作用,发现ICAM-1 的 D1 和 D2 结构域与 EGFR 的 D3 结构域之间存在潜在的相互作用。
为了进一步进行研究,作者生成了缺失构建体,研究发现了ICAM-1 的 D1 结构域与 EGFR 的 D3 结构域的潜在结合机制;通过体内验证表明 ICAM-1 的 D1 结构域是 EGFR 介导的乳腺癌细胞转移所必需的。
Fig.5 ICAM-1 D1 结构域是 EGFR 激活及其下游信号转导所必需的
作者通过中和抗体实验,发现使用中和抗体阻断 ICAM-1 可以通过抑制 EGFR/JAK1/STAT3 信号通路显著减轻乳腺癌转移。
Fig.6 使用中和抗体阻断 ICAM-1 可以抑制乳腺癌转移
研究结论
综上所述,研究阐明了 ICAM-1 作为乳腺癌转移调节因子的关键作用。
结果揭示了 ICAM-1 是 EGFR 的关键结合接头蛋白,并表明其作为 TNBC 预后标志物和治疗靶点的潜在用途。
吉满生物
如想了解更多质粒构建、病毒包装、稳转株构建、敲除细胞株、报告基因检测等相关服务。欢迎访问吉满生物官网:www.genomeditech.com 免费咨询电话:400-627-9288 原文链接: https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-024-02150-4