靶点专栏
癌症免疫疗法正在改变肿瘤治疗的格局,靶向PD-1/PD-L1免疫检查点策略的成功,展示了“治疗免疫系统而非直接治疗肿瘤”的全新理念。为克服多数患者出现的耐药性和缺乏应答性问题,目前正探索检查点抑制剂与其他免疫干预手段的联合治疗策略。
在此背景下,糖蛋白 A 重复优势蛋白(GARP)引起了广泛关注。作为潜伏型 TGF-β 的膜结合受体,GARP 能够调控 Treg 细胞及肿瘤微环境中的 TGF-β 激活,从而影响肿瘤免疫逃逸。近年来,GARP 被认为是单独使用或联合免疫检查点抑制剂的潜力靶点,有望在肿瘤免疫治疗中提供更精确、更安全的干预策略。
靶点简介
转化生长因子-β (TGFβ) 是一种具有强大免疫调节特性的多效性细胞因子,属于转化生长因子超家族。
TGF-β有三种亚型,分别为TGF-β1、TGF-β2和TGF-β3,其中TGF-β1的研究最为深入。[1] 它在免疫和干细胞调节及分化中发挥作用,是癌症、自身免疫性疾病和传染病领域研究的重点细胞因子。
糖蛋白A重复优势蛋白(GARP)又称为LRRC32, 由 Lrrc32 基因编码,是一型跨膜蛋白,分子量约 72 kDa,由 662 个氨基酸组成。
研究表明,GARP是潜在TGF-β(LTGF-β)的膜连接受体,GARP可促进LTGF-β与整合素αvβ6或αvβ8相互作用,从而触发生物活性TGF-β的释放。
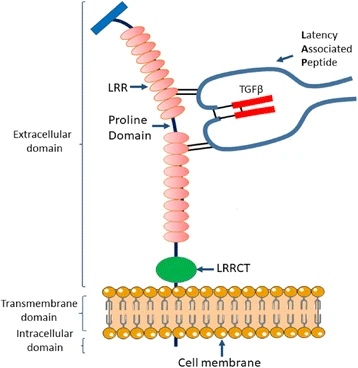
膜结合型GARP-潜伏型TGF-β1复合物的结构
免疫调控与肿瘤作用
在生理条件下,GARP广泛表达于多种细胞,尤其是在调节性T细胞(Tregs)的表达最为突出, Tregs 表面的 GARP 通过调控 TGF-β 的定位与激活,促进免疫抑制,维持免疫稳态。[2,3] 除了Tregs,GARP 还可在活化 B 细胞、血小板、间充质干细胞以及肝星状细胞表面检测到。
在肿瘤微环境中,GARP 的表达既可来源于 Tregs 和血小板,也可由肿瘤细胞本身高表达。GARP通过与LTGF-β1结合形成GARP-LTGF-β1复合物,将潜伏的 TGF-β1 富集于细胞表面,并在整合素 αvβ6等协同作用下促进成熟 TGF-β1 的释放,从而调控免疫反应。[3,4]
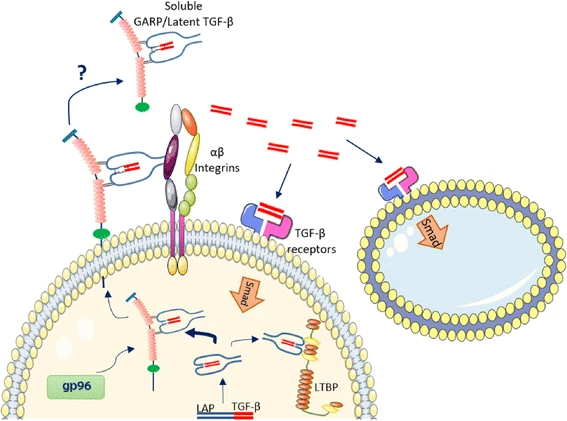
GARP参与TGF-β的成熟和激活
靶向策略与药物研发
TGF-β 信号在肿瘤发展和组织纤维化中发挥关键作用,但其广泛分布导致全身性抑制可能产生严重副作用,这限制了传统 TGF-β 抑制剂的临床应用。相比之下,GARP 在调节性 T 细胞(Tregs)、肿瘤细胞和血小板上的特异性表达,为精准阻断促肿瘤性 TGF-β 活化提供了独特机会。
目前,研究者正在探索多种基于 GARP 的干预策略:一类是直接阻断 GARP 与潜伏型 TGF-β(LTGF-β)复合物的结合,阻止成熟 TGF-β 的释放;另一类是选择性作用于 Tregs 表面的 GARP/LTGF-β 复合物,从而减弱免疫抑制而不影响效应 T 细胞功能。
现阶段在研 GARP/TGF-β1 靶向药物数量相对较少,且整体仍处于早期临床阶段,但已有产品进入临床验证,显示出一定的可行性与发展前景。
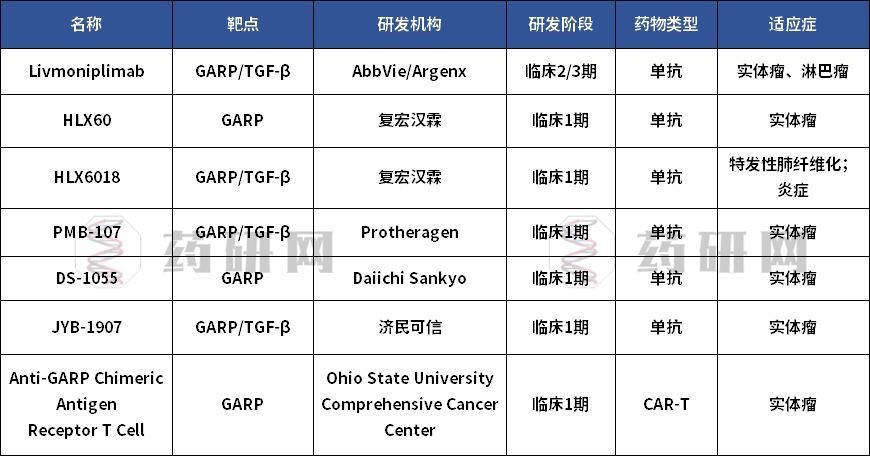
GARP/TGF-β1 靶向药物全球研发概况
小 结
GARP 靶向策略的独特优势在于,它能够在TGF-β发挥促肿瘤作用时特异性阻断其激活,同时避免全身性 TGF-β 阻断可能带来的副作用。相比传统的 Treg 清除策略(如抗 CD25 抗体),GARP 靶向策略更加精准,能够保留效应 T 细胞功能,并在肿瘤微环境中增强免疫应答。
总的来看,GARP/TGF-β1 作为新兴免疫调控靶点,在肿瘤及纤维化等疾病领域展现出良好的开发潜力。随着相关研究的持续推进,GARP 靶向药物有望为肿瘤治疗及其他免疫相关疾病提供新的研发方向和治疗选择。
用心做好细胞,为更好的靶向药
吉满生物提供 GARP/TGF-β 相关靶点研发所需的核心工具:高表达稳定细胞系、报告基因检测细胞系及阳性单克隆抗体,均经过严格功能验证,助力药物研发高效推进及临床申报(详情咨询吉满客服:18916119826)此处点击了解GARP/TGF-β 相关产品

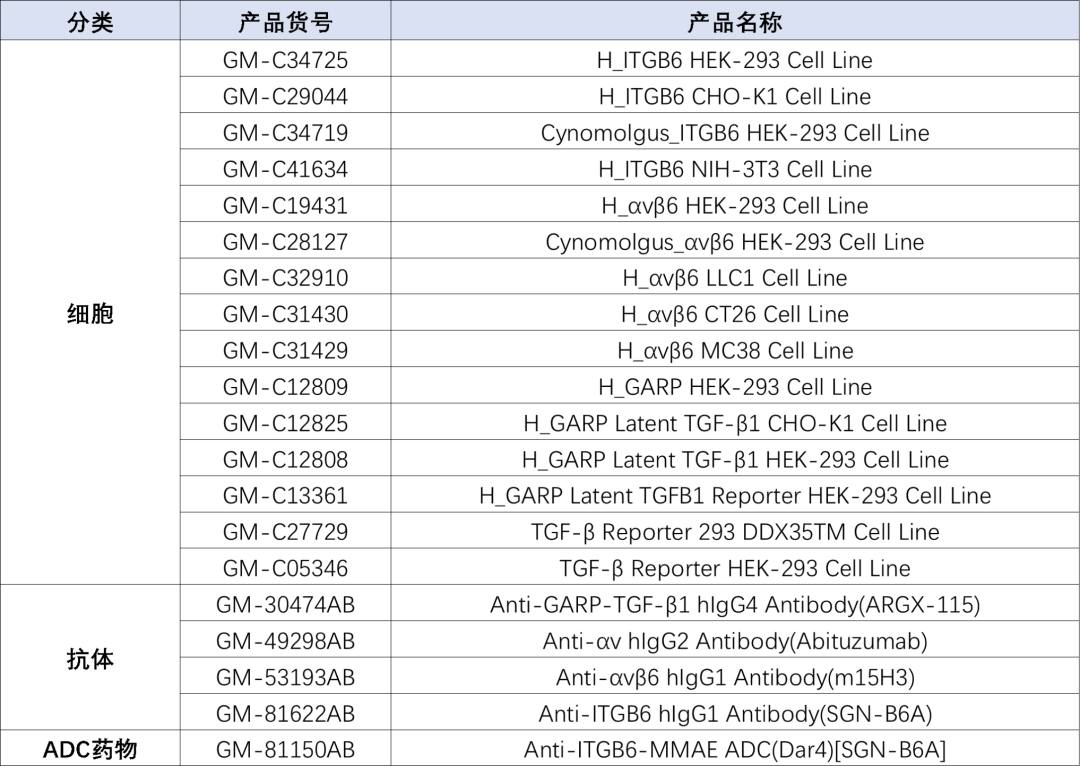
产品列表
数据展示
以下细胞系产品可高效支持 GARP- TGF-β1 靶向药物的筛选、活性评价及机制研究,为研发提供可信赖的实验工具。
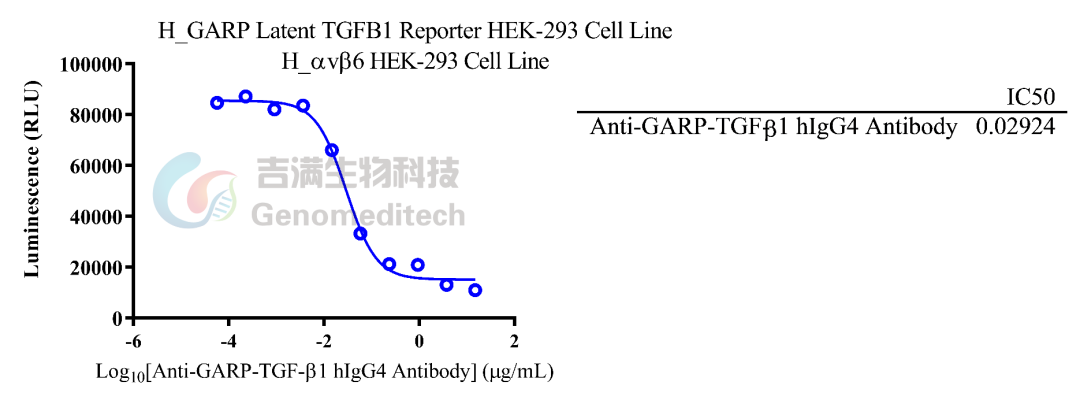
GM-C13361:H_GARP Latent TGFB1 Reporter HEK-293 Cell Line
经 Anti-GARP-TGF-β1 hIgG4 抗体(ARGX-115)阻断验证,响应稳定、结果可靠
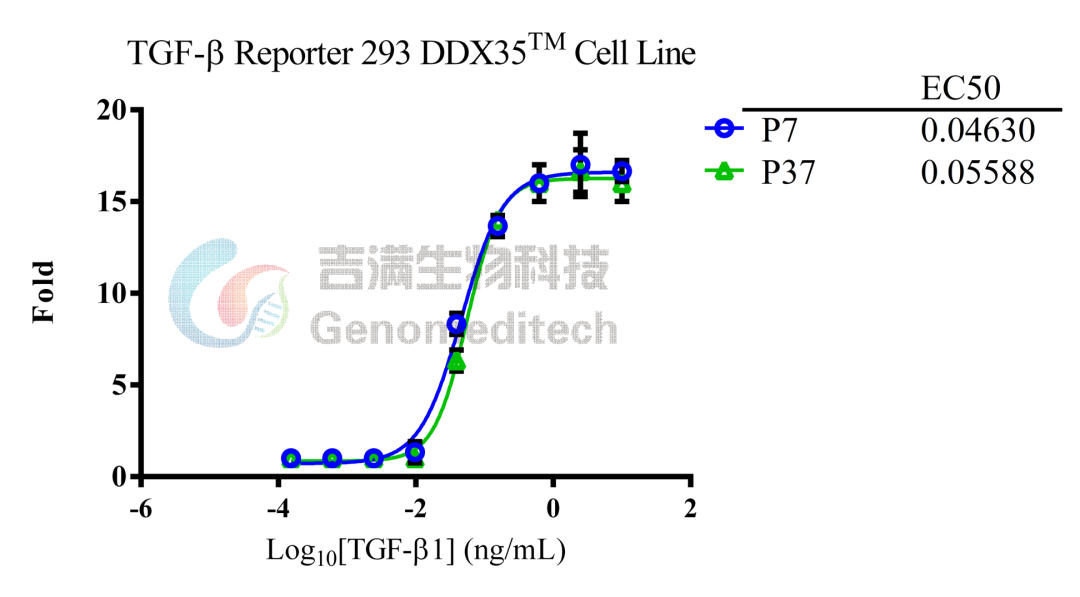
GM-C27729:TGF-β Reporter 293 DDX35TM Cell Line
经验证,细胞传代至少37代后,信号响应仍然稳定
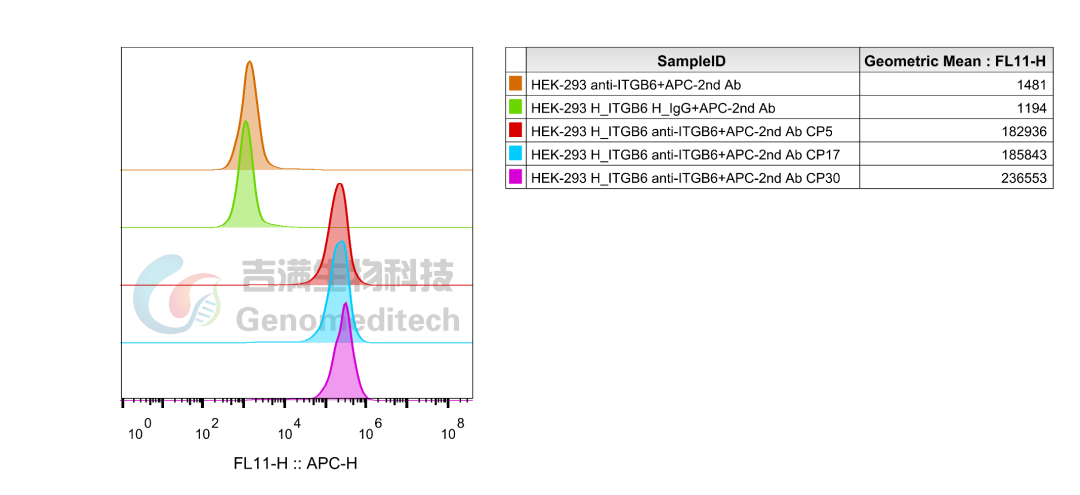
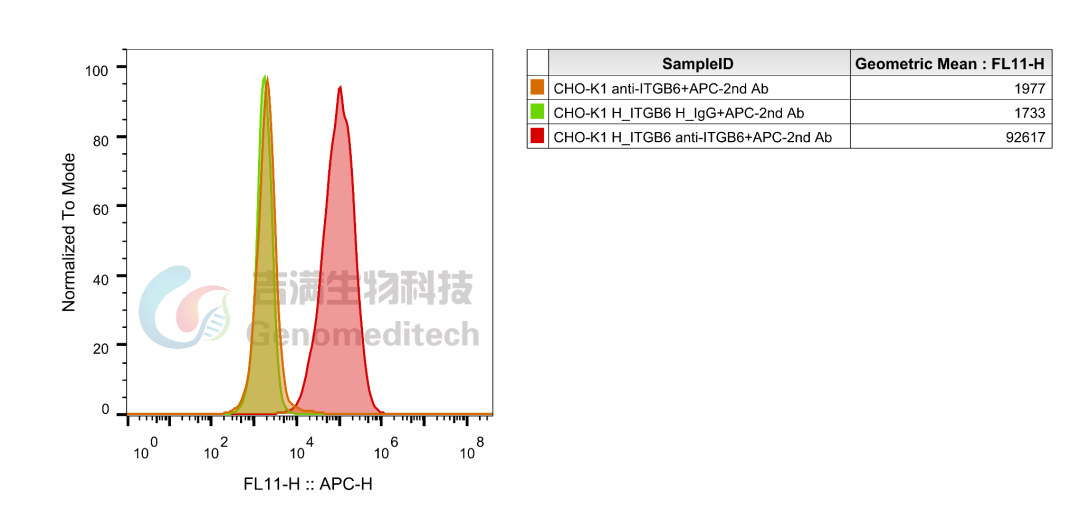
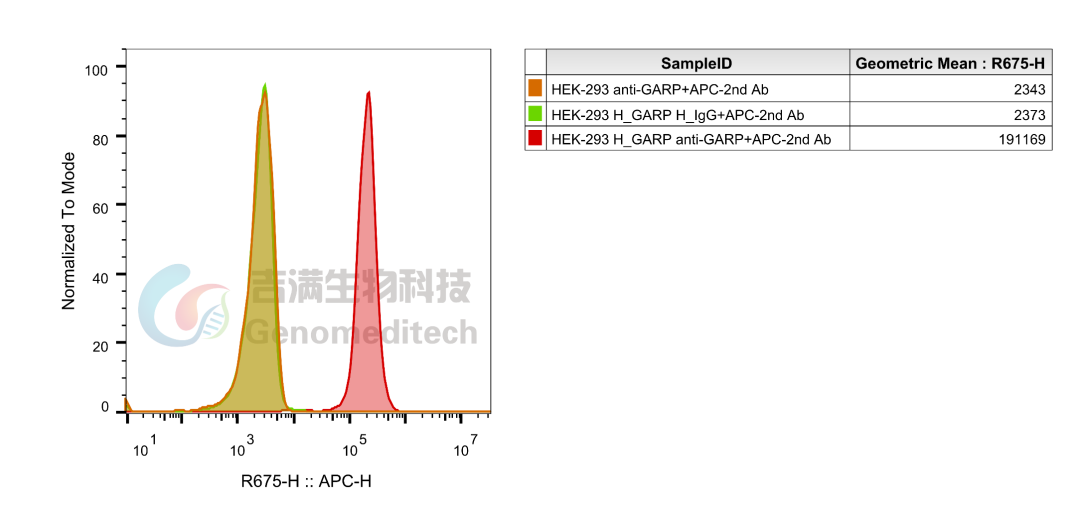
以下细胞系产品均经流式验证,表达稳定可靠,为靶向药物筛选及机制研究提供可信赖的实验工具。
GM-C34725:H_ITGB6 HEK-293 Cell Line
GM-C29044: H_ITGB6 CHO-K1 Cell Line
GM-C12809:H_GARP HEK-293 Cell Line
联系我们
吉满生物专注为生物药开发,提供高效的研发工具和解决方案。截止当前已布局近400个热门靶向药靶点,超1000株现货单克隆细胞系,涵盖肿瘤相关抗原(TAA)、 免疫检查点、Fc受体、细胞因子和激酶等热门靶点类型。旨在助力、加速大分子早期研发,做到进口细胞的国产替代。同时构建了丰富的蛋白、抗体及试剂现货产品库。
参考资料:
[1] Meng, Xiao-ming; Nikolic-Paterson, David J.; Lan, Hui Yao (June 2016). "TGF-β: the master regulator of fibrosis". Nature Reviews Nephrology. 12 (6): 325–338. doi:10.1038/nrneph.2016.48. PMID 27108839. S2CID 25871413.
[2]Tran DQ, Andersson J, Wang R, et al. GARP (LRRC32) is essential for the surface expression of latent TGF-β on activated human regulatory T cells. Proceedings of the National Academy of Sciences of the United States of America (PNAS), 2009; 106(32):13445–13450.
[3] Wang R, Kozhaya L, Mercer F, et al. Regulatory T cells promote tolerance through GARP-mediated TGF-β activation. Nature, 2009; 460: 788–792.
[4]Metelli, A., Salem, M., Wallace, C.H. et al. Immunoregulatory functions and the therapeutic implications of GARP-TGF-β in inflammation and cancer. J Hematol Oncol 11, 24 (2018). https://doi.org/10.1186/s13045-018-0570-z
[5]https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.TPS4190
[6]https://www.clinicaltrials.gov/study/NCT06109272